微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 直接排放含SO2,的烟气会形成胶雨,危害环境。利用钠碱循环法可脱除烟气中的SO2
(1)在钠碱循环法中,Na2 SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,
该反应的离子方程式是
(2)吸收液吸收SO2的过程中,pH随n(SO3²-):n(HSO3
2、选择题 下列电离方程式错误的是( ? )
A.H2CO3?2H++CO32-
B.NaHSO4(溶液)=Na++H++SO42-
C.NaHCO3=Na++HCO3-
D.CaCO3=Ca2++CO32-
3、填空题 (12分)
(1)20℃时0.1 mol・L-1NaOH分别滴定0.1 mol・L-1HCl、0.1 mol・L-1CH3COOH的pH变化曲线如下。
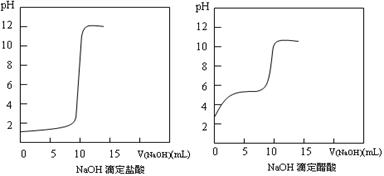
根据上述曲线回答下列问题:
①测得醋酸起点pH为3,则20℃时该浓度醋酸的电离度为 ;
②滴定开始后醋酸曲线变化比盐酸快的原因是 ;
(2)25 ℃时0.1 mol・L-1的H2R水溶液中,用氢氧化钠来调节溶液pH,得到含有H2R、HR-、R2-三种微粒的溶液。当c(Na+)=c(R2-)+c(HR-)+c(H2R)时溶液的溶质为 (填化学式)。
(3)下图是某水溶液在pH从0至14的范围内H2CO3、HCO3-、CO32-三种成分平衡时的组成分数。
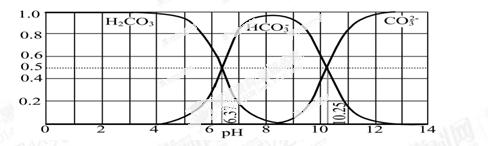
①下列叙述正确的是 。
A.此图是1.0 mol・L-1碳酸钠溶液滴定1.0 mol・L-1 HCl溶液的滴定曲线
B.在pH分别为6.37及10.25时,溶液中c(H2CO3)=c(HCO3-)=c(CO32-)
C.人体血液的pH约为7.4,则CO2在血液中多以HCO3-形式存在
D.若用CO2和NaOH反应制取NaHCO3,宜控制溶液的pH为7~9之间
(4)将尿素施入土壤后,大部分是通过转化为碳酸铵或碳酸氢铵后才被作物所利用,尿素分子在微生物分泌的脲酶作用下,转化为碳酸铵。已知弱电解质在水中的电离平衡常数(25℃)如下表:
弱电解质
| H2CO3
| NH3・H2O
|
电离平衡常数
| Ka1=4.30×10-7 Ka2=5.61×10-11
| 1.77×10-5
|
现有常温下0.1 mol・L-1的(NH4)2CO3溶液,
①你认为该溶液呈 性(填“酸”、“中”、“碱”),原因是 。
②就该溶液中粒子之间有下列关系式,你认为其中正确的是 。
A.c (NH4+)>c (CO32-)>c (HCO3-)>c (NH3・H2O)
B.c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
C.c (CO32-) + c (HCO3-) +c (H2CO3)=0.1 mol・L-1
D.c (NH4+)+ c (NH3・H2O)=2 c (CO32-) + 2c (HCO3-) +2 c (H2CO3)
4、填空题 写出下列物质在水溶液中的电离方程式:H2SO4______AlCl3______.
5、填空题 写出下列物质的电离方程式。
(1)HCl:___________。 (2)Na2SO4:________。
(3)NH4Cl:__________。 (4)Ca(OH)2:________。