��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��1����Al2��SO4��3��ȡAl��OH��3�����ð�ˮ��Al2��SO4��3��Ӧ��������NaOH��aq������ʲôԭ��? ________________________________________________________________��
��2��AlCl3��NaOH��Һ��Ӧ����Al3+��OH-�����ʵ���֮��Ϊ________ʱ������࣬________ʱ����ȫ���ܽ⣬________ʱ����Ϊ���ʱ��һ�롣
��3���ִ���ѧʵ��֤������Һ�в����ڣ�ӦΪ��Al��OH��-4�ݣ������þɵ���дϰ�ߡ���д��Al2��SO4��3��Һ�����NaOH��Һ��Ӧ�Ļ�ѧ����ʽ��������ƫ�����α�ʾ����______________________��
�ο��𰸣���1����ˮ�����NaOH��ǿ������İ�ˮ�����ܽ�Al��OH��3����������NaOH���ܽ�Al��OH��3����ʵ��������ȡAl��OH��3�ð�ˮ������NaOH
��2��1��3? 1��4? 2��3��2��7
��3��Al2��SO4��3+8NaOH�T�T2Na��Al��OH��4��+3Na2SO4
�����������2����ͼ���������з�Ӧ�õ���ͼ��
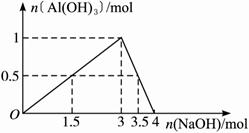
Al3++3OH-�T�TAl��OH��3��
Al3++4OH-�T�TAlO2-+2H2O
��n��AlCl3��="1" mol���ɼ���Al3+��OH-�����ʵ���֮��Ϊ1��1.5��1��3.5ʱ������Ϊ�������һ�롣
��3��д��ƫ�����ε���ʽ
Al2��SO4��3+8NaOH�T�T2NaAlO2+3Na2SO4+4H2O
����Al��OH��-4����AlO2-��2H2O����Al��OH��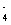 ȡ����֮�ɵô𰸡�
ȡ����֮�ɵô𰸡�
�����Ѷȣ���
2��ѡ���� �����ۺ�����������������ȼ����ֳ����ȷݣ�һ���ڸ�����ǡ����ȫ��Ӧ����������ϡ���ᷴӦ������H2aL ,��һ��ֱ�����������������Ƴ�ַ�Ӧ������ͬ�����²���H2 bL ��a�Ub����
A��1�U1
B��3�U4
C��4�U3
D��9�U8
�ο��𰸣�B
����������������ȷ�Ӧ�����ɵĽ������������ݷ�Ӧʽ8Al��3Fe3O4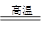 4Al2O3��9Fe��֪������9mol����Ҫ8mol��������9mol����������9mol��������8mol�����������12mol����������a�Ub��9�U12��3�U4����ѡB��
4Al2O3��9Fe��֪������9mol����Ҫ8mol��������9mol����������9mol��������8mol�����������12mol����������a�Ub��9�U12��3�U4����ѡB��
�����Ѷȣ���
3������� ����NaOH��AlCl3��MgCl2���ֹ�����ɵĻ������������ˮ�У���0.58g��ɫ�������ɣ���������Һ(�˳�0.58g����),��μ���0.5mol/L�����ᣬ�����������������ɳ�����������ͼ��ʾ[ͼ�е�Y��ʾ��������(g), x��ʾ�����������(mL)]
(1) �������NaOH������____________g(2`),
MgCl2��AlCl3�����ʵ���֮����________(2`)
(2) P������ʾ�ļ�����������Ϊ________ml.(2`)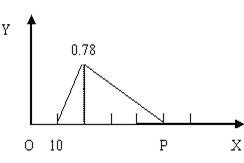
�ο��𰸣�(1)2.6g? 1:1? (2)90ml
�����������
�����Ѷȣ���
4��ѡ���� ���������м�����ϡ���ᷴӦ������������������Һ��Ӧ��
[? ]
(1)NaHCO3?(2)?(NH4)2S?(3)?Al2O3?(4)?Al?(5)?Al?(OH)3
A.(3)?(4)?
B.(3)?(4)?(5)?
C.(1)?(3)?(4)?(5)?
D.ȫ��
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5��ѡ���� ������������ʵ���Ũ�ȵ����ᡢ����������Һ�ֱ���ڼס������ձ��У�����������������������������������Ϊ5��6����ס������ձ��еķ�Ӧ��������ǣ�?��
A���ס����ж���������
B��������������������
C�����������������������
D�������������������
�ο��𰸣�B
���������������Ӧ�У�2Al+3H2SO4�TAl2��SO4��3+3H2����2Al+2NaOH+2H2O=2NaAlO2+3H2����
���ۣ���1�������������������������ȡ������������������ͬ�������������1��1��
��2������������������������ȡ���������ݷ���ʽ���������ı�ֵΪ2��3?
��3�����ڵı�ֵ��5��6����ֵ���� 2��3��1��1֮�䣬�������������������ڼ��ʱ��������������ڼ�㣬
��ѡB��
�����Ѷȣ�һ��