微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 铝及其化合物可以与盐酸和NaOH溶液反应,原因是
A.铝是活泼的金属
B.铝是不活泼金属
C.铝易发生钝化
D.铝位于金属和非金属交界线附近
参考答案:D
本题解析:根据元素周期表“位―构―性”这一特征,铝及其化合物可以与盐酸和NaOH溶液反应,原因是铝位于金属和非金属交界线附近。即选D。
点评:根据元素周期表“位―构―性”这一特征去做推断。
本题难度:一般
2、选择题 1 L某混合溶液中,溶质X、Y的浓度都为0.1 mol/L,向混合溶液中滴加某溶液Z(0.1 mol/L的氢氧化钠或硫酸溶液),所得沉淀的物质的量随着Z溶液的体积变化关系如图所示,则X、Y、Z分别是(?)
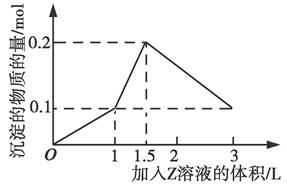
A.AlCl3、FeCl3、NaOH
B.AlCl3、MgCl2、NaOH
C.NaAlO2、Ba(OH)2、H2SO4
D.NaAlO2、BaCl2、H2SO4
参考答案:C
本题解析:若X、Y、Z分别为AlCl3、FeCl3、NaOH,则沉淀的量在加入6 L NaOH时才能达到最大值0.2 mol,A错;若X、Y、Z分别为AlCl3、MgCl2、NaOH,则沉淀的量在加入5 L NaOH时达到最大值0.2 mol,B错;若X、Y、Z分别为NaAlO2、Ba(OH)2、H2SO4,滴加硫酸时先与Ba (OH)2反应,生成BaSO4沉淀和水,然后和NaAlO2依次发生反应:AlO2-+H++H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3H2O,C正确;若X、Y、Z分别为NaAlO2、BaCl2、H2SO4,起始时即生成BaSO4沉淀和Al(OH)3沉淀,结合反应方程式知,当加入0.5 L H2SO4时,AlO2-完全反应,生成0.1 mol Al(OH)3沉淀和0.5 mol BaSO4沉淀,继续加入H2SO4,生成BaSO4沉淀的同时Al(OH)3又溶解,故沉淀的最大值不可能为0.2 mol,D错
点拨:本题考查元素化合物知识,考查考生的分析、理解能力。难度中等。
本题难度:一般
3、选择题 有200mlMgCl2、AlCl3的混合溶液,其中c(Mg2+)为0.2mol/L,c(Cl-)为1.3mol/L,要使Mg2+转化为沉淀而分离,至少需要加4mol/L NaOH溶液的体积为?(?)
A 40ml? B 72ml? C? 80ml? D 128ml
参考答案:C
本题解析:略
本题难度:简单
4、选择题 将表面已完全钝化的铝条(表面是一层Al2O3薄膜),插入下列溶液中,不会发生反应的是( )
A.稀硝酸
B.稀盐酸
C.硝酸铜
D.氢氧化钠
参考答案:氧化铝是两性氧化物,既能和强酸反应又能和强碱反应,将表面已完全钝化的铝条(表面是一层Al2O3薄膜),插入盐酸、硝酸和氢氧化钠溶液中,均会将表面的氧化膜反应掉.
故选C.
本题解析:
本题难度:一般
5、填空题 (6分)、(1)如下图横坐标为某溶液中加入溶质的物质的量,纵坐标为生成沉淀的量,若向硫
酸铝溶液中加入氢氧化钠溶液至过量,沉淀的变化符合A~C中的________
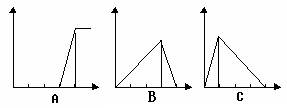
(2)现向1mol/L 100ml的AlCl3溶液中加入一定浓度的NaOH溶液100ml,充分反应后,得到3.9g沉淀,则NaOH溶液的物质的量浓度为________________________
参考答案:(6分)、(1)B? (2) 1.5mol/L或3.5mol/L?每空2分,共6分
本题解析:略
本题难度:一般