��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������Һ�и�����Ũ�ȹ�ϵ����ȷ���ǣ�������
A��0.1mol/LCH3COOH��Һ�У�c��CH3COO-��+c��CH3COOH��=0.1mol/L
B��NaHCO3��Һ�У�c��H+��+c��Na+��=2c��CO32-��+c��HCO3-��+��OH-��
C��CH3COONa��Һ�У�c��Na+����c��CH3COO-������OH-����c��H+��
D��Na2S��Һ�У�2c��Na+��=c��S2-��+c��HS-��+c��H2S��
�ο��𰸣�A��CH3COOH��Һ�и��ݴ�����غ��֪��c��CH3COO-��+c��CH3COOH��=0.1mol/L����A��ȷ��
B��NaHCO3��Һ���Ե��ԣ����������Ӵ���������������������Ӵ��ĸ������������c��H+��+c��Na+��=2c��CO32-��+
c��HCO3-��+��OH-������B��ȷ��
C��CH3COONa��Һ�У�CH3COONa�TCH3COO-+Na+������������ˮ���Լ��ԣ���c��Na+����c��CH3COO-������OH-����c��H+����ˮ��ij̶Ȳ�����c��CH3COO-������OH-������C��ȷ��
D��Na2S��Һ��n��Na��=2n��S�����������غ��֪��12c��Na+��=c��S2-��+c��HS-��+c��H2S������D����
��ѡD��
���������
�����Ѷȣ�һ��
2��ѡ���� ���ڴ�����Һ���������������?
[? ]
A.������Һ������Ũ�ȵĹ�ϵ���㣺c��H+����c��OH-��+c��CH3COO-��
B.�����¶ȣ���Һ��c(H+)/c(CH3COOH)��ֵ����
C.CH3COOH��Һ�м�������CH3COONa���壬����ĵ���ƽ�������ƶ�
D.0.10mol/L��CH3COOH��Һ�м�ˮϡ�ͣ���Һ��c��OH-����С
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3��ѡ���� ����ͬ�¶��£�100 mL0��01 mol��L��1�Ĵ�����Һ��10 mL0��1 mol��L��1�Ĵ�����Һ��Ƚϣ�������ֵǰ�ߴ��ں��ߵ���
A���к�ʱ����NaOH����
B������ij̶�
C��H�������ʵ���Ũ��
D��CH3COOH�����ʵ���
�ο��𰸣�B
���������A��100 mL0��01 mol��L��1�Ĵ�����Һ��10 mL0��1 mol��L��1�Ĵ�����Һ�к��еĴ�������ʵ�����ͬ���к�ʱ����NaOH������ͬ������B������Ũ�ȶԵ���ƽ���Ӱ����ɣ�ԽϡԽ���룬0��01 mol��L��1�Ĵ�����Һ�д������ij̶ȴ���0��1 mol��L��1�Ĵ�����Һ�д���ĵ���̶ȣ���ȷ��C��H�������ʵ���Ũ�ȣ�ǰ��С�ں��ߣ�����D��������Һ��CH3COOH�����ʵ�����ȣ�����
�����Ѷȣ�һ��
4��ѡ���� �����£���l00mL 0��01 mol?L-1��������μ���0��02 mol?L-1 MOH��Һ������ͼ��ʾ�����߱�ʾ�����Һ��pH�仯�������Һ����仯���Բ��ƣ�������˵���в���ȷ���ǣ�?��
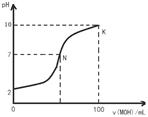
A��MOH������
B��N��c(Cl-) = c(M+)
C������MOH��Һ�ĵμӣ���ֵ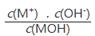 ����
����
D��K���Ӧ����Һc(MOH)+c(OH-)��c(H+) = 0��005 mol?L-1
�ο��𰸣�D
���������A�� ��MOHΪǿ�����ǡ����ȫ�к�ǰ����Һ��pHӦ����һ���ܴ��ͻԽ�������Ǹ�ͼ��pH��ǡ���к�ʱ�仯�����ԡ����MOHΪ�����ȷ��B�����ݵ���غ�ɵ�c(Cl-)+c(OH-) = c(H+)+c(M+),����N�����Һ��c(OH-) = c(H+)������N��c(Cl-) = c(M+)����ȷ��C������MOH��Һ�ĵμӣ�c(M+)��c(OH-)����������ǡ����ȫ�к�ǰ�� c(MOH)��С�����c(M+)��c(OH-)/ c(MOH)��ֵ��������D����K����ݵ���غ�ɵ�c(H+)+c(M+)=c(OH-)+c(Cl-);���������غ�ɵ�c(M+)+ c(MOH) =0��01 mol/L��c(Cl-)=0��005mol/L������c(M+)=c(OH-)+c(Cl-)- c(H+)��c(M+)+ c(MOH)= c(OH-)+c(Cl-)- c(H+)+ c(MOH)��c(MOH)+c(OH-)��c(H+) = 0��01mol/L-0��005mol/L=0��005mol/L����ȷ��
�����Ѷȣ�һ��
5������� ��10�֣����г����µ������Һ��
��0.01 mol��L��1 CH3COOH��Һ�� ��0.01 mol��L��1 HCl��Һ��
��pH��12�İ�ˮ�� ��pH��12��NaOH��Һ��
��0.01 mol��L��1 HCl��Һ��pH��12��NaOH��Һ��������������Һ��
��1������ˮ�ĵ���̶�������______(����ţ���ͬ)��ˮ�ĵ���̶���ͬ����______��
��2�������ڡ��ۻ�Ϻ�������ҺpH��7����������Һ���������________��(�����������������)��
��3����ǰ�ķ���Һͬ��ϡ��10������Һ��pH��
��________�ڣ���________�� (�����������������)��
�ο��𰸣���1���� �ڢۢ� ��2���� ��3��> ��
�����������1����0.01 mol��L��1 HCl��Һ��pH��12��NaOH��Һ�������ϣ�ǡ�÷�Ӧ��������Һ���Ȼ�����Һ��ǿ��ǿ���Σ���ˮ�ĵ���û��Ӱ�죬�٢ڢۢ����������ˮ�ĵ������������ã���������ˮ�ĵ���̶������Ǣݣ��ڢۢ���Һ��ǿ�ᡢ���ǿ���Һ�������Ӻ�����������Ũ����ͬ����ˮ�ĵ������Ƴ̶���ͬ����ˮ�ĵ���̶���ͬ���Ǣڢۢܣ�(2 ) �ڢ����������Ϻ���Һ�ʼ��ԣ���ʹ��ҺpH=7����������Һ��������ڣ��� ����3�� ͬŨ�ȴ��������ϡ����ͬ������Ũ����Ȼ��ͬ����������ڵ���ƽ�⣬������Һ��������Ũ��С��������Һ�е�������Ũ�ȣ�����Խ����pHԽ��������ҺPH�٣��ڣ�PHֵ��ͬ�İ�ˮ���������ƣ�ϡ����ͬ�ı�������ˮ�������룬��Һ������������Ũ�ȴ�������������Һ�����������ӣ�pHֵ�ۣ��ܡ�
���㣺����������ʵĵ���ƽ�⡣
�����Ѷȣ�һ��