微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 X、Y为短周期元素,X位于IA族,X与Y可形成化合物X2Y,下列说法不正确的是( )
A.两元素形成的化合物中原子个数比可能为1:1
B.X与Y的简单离子可能具有相同电子层结构
C.X的原子半径一定大于Y的原子半径
D.X2Y可能是离子化合物,也可能是共价化合物
参考答案:X、Y为短周期元素,X位于IA族,则X可能是H、Li、Na元素,X与Y可形成化合物X2Y,该化合物中X显+1价,则Y显-2价,则Y是第VIA族元素,为O或S元素,
A.H或Na与O元素形成H2O2或Na2O2时,X和Y的原子个数比是1:1,故正确;
B.当X是Na元素,Y是O元素时,钠离子和氧离子的电子层结构相同,故正确;
C.当X为H原子,Y为O或S原子时,X的原子半径小于Y,故C错误;
D.X2Y是Na2O或Na2S是离子化合物,X2Y是H2O或H2S是共价化合物,故正确;
故选C.
本题解析:
本题难度:简单
2、选择题 有关化学用语正确的是( )
①羟基的电子式?
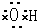
?②乙烯的结构简式:CH2CH2]③硫化氢的电子式
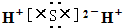
?④丙烷分子的球棍模型:
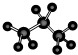
⑤苯分子的比例模型?

?⑥甲烷的结构式?
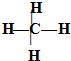
A.①④
B.②③④
C.④⑤⑥
D.②③⑤
参考答案:C
本题解析:
本题难度:简单
3、选择题 近期报道,中国科学家以二氧化碳为碳源,金属钠为还原剂,在470℃、80Mpa下合成出金刚石,具有深远意义。下列说法不正确的是
[? ]
A.由二氧化碳合成金刚石是化学变化
B.金刚石是碳的一种同位素
C.钠被氧化最终生成碳酸钠
D.金刚石中只含有非极性共价键
参考答案:B
本题解析:
本题难度:简单
4、填空题 【化学―物质结构与性质】(15分)
许多金属及它们的化合物在科学研究和工业生产中具有许多用途.回答下列有关问题:
(1)基态Ni核外电子排布式为________________, 第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是________________;
(2)①已知CrO5中Cr为+6价,则CrO5的结构式为 ??。
②金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n ,与Ni(CO)n中配体
互为等电子体的离子的化学式为?(写出一个即可)。
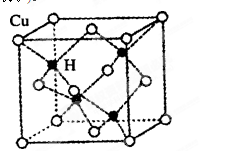
③铜是第四周期最重要的过渡元素之一,其单质及化合物有广泛用途。已知CuH晶
体结构单元如图所示。该化合物的的密度为ρg/cm3,阿伏加德罗常数的值为NA,则
该晶胞中Cu原子与H原子之间的最短距离为?cm(用含ρ和NA的式子表示)。
(3)另一种铜金合金晶体具有面心立方最密堆积的结构,在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为__________,若该晶胞的边长为a pm,则合金的密度为_________ g・cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
参考答案:(15分)(1)1s22s22p63s23p6 3d84s2 (2分)?C(碳)(2分)
(2) ①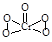 (2分) ②? CN-(C22- 、O22+)(2分)
(2分) ②? CN-(C22- 、O22+)(2分)
③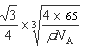 (2分)
(2分)
(3) 1∶3(2分)? (197+64×3) ×1030/(a3NA)(3分)
本题解析:(1)基态Ni是28号元素,改进核外电子的排布原理,其核外电子排布式为1s22s22p63s23p6 3d84s2;Ni原子中有2个未成对电子,第二周期中有2个未成对电子的是C或O,其中电负性最小的是C;
(2)①已知CrO5中Cr为+6价,Cr原子周围5个O原子,说明Cr与1个O原子是双键结合其余为单键,O原子成2个共价键,所以CrO5结构式为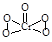 ;
;
②Ni(CO)n中配体是CO,是2原子10个价电子的分子,与它是等电子体的离子有CN-(C22- 、O22+);
③ CuH晶胞中有4个Cu原子和4个H原子,设晶胞棱长为acm,则4×65/NA/a3=ρg/cm3,则a3=4×65/ρ NA该晶胞中Cu原子与H原子之间的最短距离为以4个Cu原子为顶点H原子为中心的正四面体的中心到顶点的距离,正四面体的棱长为面对角线的一半即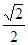 a,利用数学知识可求正四面体的中心到顶点的距离为
a,利用数学知识可求正四面体的中心到顶点的距离为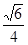 ×
×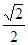 a=
a=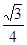 a=
a=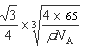 ;
;
(3)位于顶点的原子是该晶胞的1/8,所以顶点上的Au原子的个数是8×1/8=1,位于面心的原子属于该晶胞的1/2,所以Cu原子的个数为6×1/2=3,则该合金中Au原子与Cu原子个数之比为1:3;1pm=1×10-10cm,所以该合金的密度是(197+3×64)/ NA/(a×10-10)3=(197+64×3) ×1030/(a3NA)。
本题难度:一般
5、简答题 图为周期表中短周期的一部分.已知a原子的最外层上的电子数目是次外层电子数目的一半,下列说法中不正确的是( )
A.元素a的最高价氧化 物的水化物的酸性比b弱
B.元素a的原子半径比d的大
C.元素a的单质在空气中燃烧会导致“温室效应”
D.元素a单质是一种良好的半导体材料