微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在KMnO4中,Mn的化合价是( ? )
A.+2
B.+4
C.+6
D.+7
参考答案:D
本题解析:
本题难度:简单
2、简答题 按要求填空:
(1)羟基的电子式是______;
(2)给下列有机物命名:
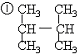
______
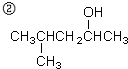
______
(3)2-甲基-1,3-丁二烯的键线式______;
(4)
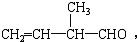
所含官能团的名称是______;该有机物发生加聚反应后,所得产物的结构简式为______.
参考答案:(1)氧原子与氢原子通过一对共用电子对连接,羟基中的氧原子含有一个未成对电子,电子式为:
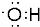
故答案为:
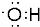
(2)根据有机物的命名原则
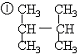
名称为:2,3-二甲基丁烷
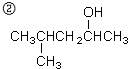
名称为:4-甲基-2-戊醇
故答案为:2,3-二甲基丁烷;4-甲基-2-戊醇
(3)2-甲基-1,3-丁二烯的结构简式为
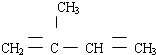
所以键线式为
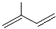
.
故答案为:

(4)
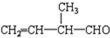
含官能团的名称是碳碳双键,醛基;
发生加聚反应为n
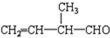
一定条件
本题解析:
本题难度:一般
3、填空题 (每空2分,共12分)键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。参考以下表格的键能数据,回答下列问题:
化学键
| Si―O
| Si―Cl
| H―H
| H―Cl
| Si―Si
| Si―C
|
键能/kJ・mol-1
| 460
| ? 360
| 436
| 431
| 176
| 347
|
?
(1)比较下列两组物质的熔点高低(填“>”或“<”)
SiC ?Si; SiCl4?SiO2
(2)能不能根据键能的数据判断单质Si 和化合物SiCl4的熔点高低??(填“能”或“不能”),原因是?。
(3)如图立方体中心的“・ ”表示金刚石晶体中的一个原子,请在立方体的顶点用“・ ”表示出与之紧邻的碳原子
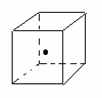
(4)工业上高纯硅可通过下列反应制取:SiCl4(g) + 2H2(g)?高温??Si(s)+4HCl(g)
计算该反应的反应热△H为__________________。
参考答案:(1)>,<?
(2)不能,物质熔点高低由构成物质的微粒间作用力决定,单质Si属于原子晶体,原子间作用力是共价键;SiCl4属于分子晶体,分子间作用力是范德华力,比共价键弱得多。因此不能都根据键能来判断物质的熔点高低。?
(3)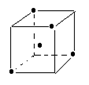 ?
?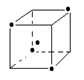 (4)+236 kJ/mol?)
(4)+236 kJ/mol?)
本题解析:(1)碳化硅和硅都是原子晶体,其熔点大小和共价键强弱有关系。形成共价键的原子半径越小,共价键越强,碳原子半径小于硅原子的,所以碳化硅的熔点高于硅放的。四氯化硅是分子晶体,二氧化硅是原子晶体,所以四氯化硅的熔点小于二氧化硅的。
(2)由于物质熔点高低由构成物质的微粒间作用力决定,单质Si属于原子晶体,原子间作用力是共价键;SiCl4属于分子晶体,分子间作用力是范德华力,比共价键弱得多。因此不能都根据键能来判断物质的熔点高低。
(3)金刚石中每一个碳原子与周围的4个碳原子连接,构成正四面体,所以结构如图。
(4)反应热就是断键吸收的能量和形成化学键所放出的能量的差值,因此反应热是360 kJ/mol×4+436 kJ/mol×2-176 kJ/mol×2-431 kJ/mol×4=+236 kJ/mol。
本题难度:一般
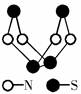
4、选择题 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。其中下图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是(?)
A.该物质的分子式为SN
B.该物质的分子中既有极性键又有非极性键
C.该物质具有很高的熔、沸点
D.该物质与化合物S2N2互为同素异形体
参考答案:B
本题解析:根据分子结构可知,分子式为S4N4,所以A不正确。根据结构可判断,硫和硫之间形成非极性键,S和N之间形成极性键,B正确。该物质形成的晶体是分子晶体,熔沸点不是很高,C不正确。由同一种元素形成的不同单质互为同素异形体,该物质是化合物,不是单质,D不正确,答案选B。
本题难度:一般
5、选择题 下列四种元素中,其单质氧化性最强的是( )
A.原子含未成对电子最多的第二周期元素
B.原子最外层电子排布为2s22p4的元素
C.位于周期表中第三周期ⅢA族的元素
D.原子最外层电子排布为3s23p3的元素
参考答案:A、原子含未成对电子最多的第二周期元素是N元素,氮气的化学性质稳定;
B、原子最外层电子排布为2s22p4的元素是O元素,
C、位于周期表中第三周期ⅢA族的元素是Al元素,
D、原子最外层电子排布为3s23p3的元素是P元素,
非金属性O>N>P,氧气的氧化性最强,
故选B.
本题解析:
本题难度:简单