微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 A、B、C都是金属,A和C分别放入同浓度的稀硫酸中,A的反应速率比C快,A与B和硫酸铜溶液组成原电池时,A的质量增加.A、B、C三种金属的活动性顺序为( )
A.A>B>C
B.A>C>B
C.B>A>C
D.C>A>B
参考答案:A、B、C都是金属,相同条件下,金属性越强的金属置换出氢气的反应速度越快,A和C分别放入同浓度的稀硫酸中,A的反应速率比C快,所以A的金属性比C强;
原电池放电时,较活泼金属作负极,负极上金属失电子生成金属阳离子进入溶液,导致负极质量减少,正极上溶液中铜离子得电子生成铜单质,导致正极质量增加,A与B和硫酸铜溶液组成原电池时,A的质量增加,A做正极,B作负极,所以B的金属性比A强,所以A、B、C三种金属的活动性顺序为B>A>C.
故选C.
本题解析:
本题难度:一般
2、选择题 根据下图,下列判断中正确的是
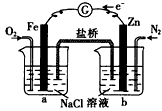
[? ]
A.烧杯a中的溶液pH 升高
B.烧杯b中发生氧化反应
C.烧杯a中发生的反应为2H++2e-=H2
D.烧杯b中发生的反应为2Cl--2e-=Cl2
参考答案:AB
本题解析:
本题难度:一般
3、填空题 煤制备CH4是一种有发展前景的新技术。
I. 煤炭气化并制备CH4包括以下反应:
C(s)+H2O(g)=CO(g)+H2 (g) ΔH 1 = +131 kJ/mol
CO(g) + H2O(g)=CO2 (g)+ H2(g) ΔH 2 = ?41 kJ/mol
CO(g) + 3H2 (g)=CH4 (g)+ H2O(g) ΔH 3 = ?206 kJ/mol
(1)写出煤和气态水制备CH4(产物还有CO2)的热化学方程式 。
(2)煤转化为水煤气(CO和H2)作为燃料和煤直接作为燃料相比,主要的优点有 。
(3)写出甲烷―空气燃料电池(电解质溶液为KOH溶液)中负极的电极反应式 。
II. 对以上反应CO(g) + H2O(g)  CO2 (g)+ H2(g) ΔH 2 = ?41 kJ/mol,起始时在密闭容器中充入1.00 molCO和1.00 molH2O,分别进行以下实验,探究影响平衡的因素(其它条件相同且不考虑任何副反应的影响)。实验条件如下表:
CO2 (g)+ H2(g) ΔH 2 = ?41 kJ/mol,起始时在密闭容器中充入1.00 molCO和1.00 molH2O,分别进行以下实验,探究影响平衡的因素(其它条件相同且不考虑任何副反应的影响)。实验条件如下表:
实验编号
| 容器体积/L
| 温度/°C
|
①
| 2.0
| 1200
|
②
| 2.0
| 1300
|
③
| 1.0
| 1200
|
(1)实验①中c(CO2)随时间变化的关系见下图,请在答题卡的框图中,画出实验②和③中c(CO2)随时间变化关系的预期结果示意图。
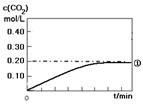
(2)在与实验①相同的条件下,起始时充入容器的物质的量:n(CO)=n(H2O)=n(CO2) =n( H2)=1.00mol。通过计算,判断出反应进行的方向。(写出计算过程。)
参考答案:I.(1)2C(s)+ 2H2O(g)= CH4 (g)+ CO2 (g) ΔH = +15 kJ/mol (3分 )
(2)提高煤的利用率(节约能源或节约资源)(1分)、减少污染。(1分)
(3)CH4―8e-+10OH-=CO32-+7H2O(2分)
II. (1) 如图所示
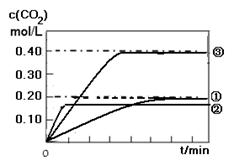
(2)Q> K 反应向逆反应方向(生成CO和H2O的方向)进行 (1分)
本题解析: I. (1) 根据盖斯定律和已知方程式,煤和气态水制备甲烷的热化学方程式可由方程式①×2+②+③而得,所以ΔH=2ΔH 1+ ΔH 2+ΔH 3 = +15 kJ/mol ,所以热化学方程式为:2C(s)+ 2H2O(g)= CH4 (g)+ CO2 (g) ΔH = +15 kJ/mol 。
(2) 煤气化后生成水煤气再燃烧比直接燃烧煤更加充分,提高能源利用率,同时燃煤容易产生酸雨,所以燃烧水煤气还可以减少污染。
(3)用甲烷作燃料制成的碱性燃料电池中,甲烷失电子生成的CO2气体会与溶液中的碱性介质进一步反应生成CO32-,所以其负极的反应式为:CH4―8e-+10OH-=CO32-+7H2O。
II. (1) CO(g) + H2O(g)  CO2 (g)+ H2(g) 的反应是一个放热反应,所以温度升高,反应的反应速率加快,但使平衡逆向移动,实验②曲线比实验①曲线更快达到平衡,但是平衡时CO2的浓度要低一些;相比之下,实验③比试验①缩小了体积,即增大了压强,由于反应前后气体系数不变,所以增大压强只能增大化学反应速率,但是不能改变平衡,因此实验③的曲线比实验①更快达到平衡,且平衡时CO2的浓度是实验①的2倍。如图
CO2 (g)+ H2(g) 的反应是一个放热反应,所以温度升高,反应的反应速率加快,但使平衡逆向移动,实验②曲线比实验①曲线更快达到平衡,但是平衡时CO2的浓度要低一些;相比之下,实验③比试验①缩小了体积,即增大了压强,由于反应前后气体系数不变,所以增大压强只能增大化学反应速率,但是不能改变平衡,因此实验③的曲线比实验①更快达到平衡,且平衡时CO2的浓度是实验①的2倍。如图

(2)整体思路:先根据实验①充入的物质的物质的量和平衡时候CO2的浓度计算出在相同温度下的平衡常数K,然后比较此时的浓度商Q与实验①的K值的大小,从而得出反应进行的方向。
计算过程为:
(2) 平衡时n(CO2)=0.20mol/Lx2.0L=0.40mol
CO(g) + H2O(g) 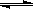 CO2 (g)+ H2(g)
CO2 (g)+ H2(g)
起始物质的量/mol 1.00 1.00 1.00 1.00
变化物质的量/mol 0.40 0.40 0.40 0.40
平衡物质的量/mol 0.60 0.60 0.40 0.40 (1分)
K=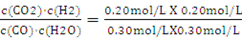 ="0.44" (2分)
="0.44" (2分)
Q=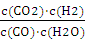 =
=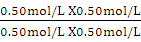 =" 1.0" (1分)
=" 1.0" (1分)
Q> K 反应向逆反应方向(生成CO和H2O的方向)进行 (1分)
考点:本题考查的是化学反应原理知识,主要包括盖斯定律应用、热化学方程式的书写、影响化学平衡的因素、图像问题、反应方向的判断计算。
本题难度:困难
4、选择题 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
A.充电时阳极反应为Zn-2e-+2OH-=Zn(OH)2
B.充电时OH-向阳极移动
C.放电时每转移3 mol e-正极有1 mol K2FeO4被氧化
D.充电时,电源的正极应与电池的Zn(OH)2极相连
参考答案:B
本题解析:A项,通过总反应可以判断该反应为放电时负极发生的反应;B项,充电时阴离子向电解池的阳极移动;C项,正极得电子,化合价降低,被还原;D项,电池的Zn(OH)2极充电 91Exam.org时为阴极,应与电源的负极相连。
点拨:本题考查蓄电池,考查考生书写电极反应式的能力。难度中等。
本题难度:一般
5、选择题 关于下图所示装置,下列叙述中正确的是

A.铜是负极,锌片上有气泡产生
B.锌片逐渐减轻,铜片逐渐增重
C.电流从锌片经导线流向铜片
D.氢离子在铜片表面得电子被还原
参考答案:D
本题解析:A 错误,铜是正极,铜片上有气泡产生
B 错误,铜片质量不变
C 错误,电子从锌片经导线流向铜片
D 正确。
本题难度:简单