微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 阿波罗宇宙飞船上使用的是氢-氧燃料电池,其电极总反应式为:2H2+O2=2H2O;电解质溶液为KOH溶液,反应保持在较高温度,使水蒸发,下列叙述正确的是( )
A.此电池能见到浅蓝色火焰
B.H2为正极,O2为负极
C.工作时电解液的pH不断增大
D.电极反应为:负极2H2+4OH--4e-=4H2O正极O2+2H2O+4e-=4OH-
2、填空题 (12分)火力发电厂释放出大量的氮氧 化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g)△H1=-574 kJ・mol-1
CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2 O(g)△H2=-1160 kJ・mol-1
O(g)△H2=-1160 kJ・mol-1
甲烷直接将NO2还原为N2的热化学方程式为?。
 (2)脱碳。将CO2转化为甲醇的热化学方程式为:
(2)脱碳。将CO2转化为甲醇的热化学方程式为:
CO2(g)+3H2(g)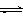 CH3OH(g)+H2O(g)?△H3
CH3OH(g)+H2O(g)?△H3
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图1所示,则上述CO2转化为甲醇的反应的△H3?0(填“>”、“<”或“=”)。

②在一恒温恒容密闭容 器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如图2所示。下列说法正确的是?(填字母代号)。
器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如图2所示。下列说法正确的是?(填字母代号)。
A.第10 min后,向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时c(CH3OH)="1.5" mol/L
B.0~10 min内,氢气的平均反应速率为0.075 mol/(L・min)
C.达到平衡时,氢气的转化率为0.75
D.升高温度将使n(CH3OH)/n(CO2)减小