| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点归纳《物质的量》高频试题预测(2017年最新版)(六)
参考答案:D 本题解析:A选项中,己烷在标准状态下不是体态,所以不能用22.4L计算物质的量。B选项NA个分子,则混合气体为1mol,而每个分子中都有两个氧原子,所以氧原子为2mol,数目为2NA。C选项中常温常压下的氯气不能计算氯气的物质的量,无法分析是否过量,D正确。 本题难度:困难 4、选择题 由CO2、H2和CO组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中CO2、H2和CO的体积比为( ) |
参考答案:C
本题解析:
试题解析:同温同压下,气体摩尔体积相等,根据ρ=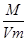 知,CO2、H2和CO组成的混合气体平均摩尔质量与氮气摩尔质量相等,M(N2)=M(CO)=28g/mol,所以混合气体平均摩尔质量与CO多少无关,则CO2、H2的平均摩尔质量为28g/mol,设CO2、H2的物质的量分别是x、y,平均摩尔质量M=
知,CO2、H2和CO组成的混合气体平均摩尔质量与氮气摩尔质量相等,M(N2)=M(CO)=28g/mol,所以混合气体平均摩尔质量与CO多少无关,则CO2、H2的平均摩尔质量为28g/mol,设CO2、H2的物质的量分别是x、y,平均摩尔质量M=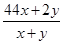 g/mol
g/mol
=28g/mol,故x:y=13:8。根据V=nVm知,相同条件下,不同物质的量的气体体积之比等于其物质的量之比,所以三种气体的体积之比可以是13:8:29。
考点:阿伏加德罗定律及推论
本题难度:一般
5、选择题 下列叙述中正确的是( )
A.标准状况下,22.4L水的物质的量为1mol
B.常温常压下,16g氧气中约含有2NA个氧原子
C.25℃时,1L1mol?L-1的氢氧化钠溶液的质量为40g
D.0.5molCH4中约含有5NA个电子
参考答案:A.标况下,水为液态,不能使用气体摩尔体积计算其物质的量,22.4L水的物质的量原大于1mol,故A错误;
B.氧气分子由氧原子构成,16g氧气中O原子的物质的量=16g16g/mol=1mol,故含有O原子数目为NA,故B错误;
C.1L1mol?L-1的氢氧化钠溶液中溶质NaOH的质量=1L×1mol/L×40g/mol=40g,而溶液的质量=溶质质量+溶剂质量,溶液的质量大于40g,故C错误;
D.1个CH4分子含有10个电子,电子物质的量=0.5mol×10=5mol,含有电子数目=5mol×NAmol-1=5NA,故D正确,
故选D.
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《物质的分离.. | |