��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� AԪ�ص������ӡ�BԪ�ص������Ӻ�CԪ�ص������Ӿ�����ͬ�ĵ��Ӳ�ṹ����֪A��ԭ����������B��ԭ����������A��B��C�������Ӱ뾶��С��˳����
A. C��B��A?B. C��A��B? C.A��B��C?D. B��A��C
�ο��𰸣�D
���������AԪ�ص������ӡ�BԪ�ص������Ӻ�CԪ�ص������Ӿ�����ͬ�ĵ��Ӳ�ṹ����AB�Ƿǽ�����C�ǽ�����λ��AB����һ���ڡ���������Ų���ͬ�����������뾶��ԭ���������������С����A��B��C�������Ӱ뾶��С��˳����B��A��C����ѡD��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������ǿ�����ض�ѧ��������û���֪ʶ���ʵ�����������������������������ѧ������˼ά�����ͷ�ɢ˼ά������
�����Ѷȣ�һ��
2��ѡ���� X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ��е�λ����ͼ��ʾ����Yԭ�ӵ������������Ǵ�����������3��������˵������ȷ����
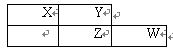
A��W��������ˮ��Ӧ������һ�־���Ư���Ե�����
B��ԭ�Ӱ뾶��W��Z��Y��X
C��4��Ԫ�صĵ����У�Z���ʵ��ۡ��е����
D������������Ӧˮ���������:Z��W��X
�ο��𰸣�A
�����������
�����Ѷȣ���
3��ѡ���� ���й���Ԫ�����ڱ���˵����ȷ����
A��Ԫ�����ڱ��ǰ���Ԫ�����ԭ��������С���ж��ɵ�
B��Ԫ�����ڱ���7�����У�Ҳ��7�����ڣ���18�����У���18����
C������λ��Ԫ�����ڱ���ͬһ���ڵ�Ԫ�أ����ǰ������ҵ�˳��ԭ��������������1������8
D������λ��Ԫ�����ڱ���ͬһ�����Ԫ�أ����ǰ����ϵ��µ�˳����Ӳ���������
�ο��𰸣�D
������������⿼��Ԫ�����ڱ��Ľṹ������
Ԫ�����ڱ��ǰ���Ԫ�ص�ԭ�������Ĵ�С���ж��ɵģ���A����
Ԫ�����ڱ���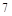 �����ڣ�
�����ڣ�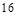 ���壬��B����
���壬��B����
����λ��Ԫ�����ڱ���ͬһ���ڵ�Ԫ�أ����Ӳ�������ͬ�������ڵ�Ԫ�ش����ҵ�˳��ԭ��������������1������8����������Ԫ���˽��ۣ���C��
����λ��Ԫ�����ڱ���ͬһ�����Ԫ�أ����ǰ����ϵ��µ�˳����Ӳ��������࣬D��ȷ
����ȷ��Ϊ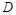
�����Ѷȣ�һ��
4��ѡ���� ������Ԫ���γɵ�3������Xn+��Ym-��Zm+����֪m��n��Xn+��Zm+��һ�����Ӳ㣬Z��Yͬ���ڣ�����ԭ�ӵ�M���������Ϊż���������ƶϲ���ȷ����
A��ԭ�Ӱ뾶X��Y��Z
B�����Ӱ뾶Ym-��Xn+��Zm+
C������Ԫ������������Ӧˮ����������μ���������������ǿ��˳����X��Z��Y
D��Y����Ȼ����û������̬�����γ�ԭ�Ӿ���
�ο��𰸣�A��D
���������
�����⣬��ȷ������Ԫ�������ڱ��е����λ��Ϊ��
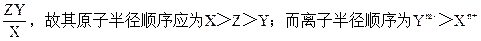
��Zm+������Ԫ�ذ�X��Z��Y˳������Լ������ǽ�������ǿ����C������Ҳ����ȷ�ģ���ΪY�����γ�Ym-���ӣ���Y�������γ�ԭ�Ӿ��塣
�����Ѷȣ�һ��
5������� ����Ԫ�����ڱ�1~20��Ԫ�ص����ʺ͵ݱ����,�ش��������⡣
(1)���ڽ���Ԫ�ص�������������,��������ǿ��Ԫ����������Ӧ���ɵĻ���������������(�����ֻ�����Ļ�ѧʽ)��?
(2)����ϡ�����������������(��Ԫ�ط���,��ͬ)��?
(3)�γɻ�����������������Ԫ��������?
(4)����������,ԭ�Ӱ뾶������(ϡ���������)����������?
(5)�Ʋ�Si��N����⻯����ȶ�����������������������(�ѧʽ)��?
�ο��𰸣�(1)7��K2O��K2O2(KO2Ҳ����)
(2)He��Ne��Ar
(3)C��H
(4)Na
(5)NH3��SiH4
���������ǰ20��Ԫ����,(1)���ڽ���Ԫ�صĹ���7��,���н�������ǿ��Ԫ���Ǽ�,����������Ӧ���ɵĻ�������K2O��K2O2��KO2��;(2)����ϡ���������He��Ne��Ar;(3)�γɻ�����������������Ԫ����C��H;(4)ͬһ����,��ԭ����������ԭ�Ӱ뾶��С,�ʵ���������,ԭ�Ӱ뾶������Na;(5)�ǽ�����:N>P>Si,��NH3���ȶ��Դ���SiH4���ȶ��ԡ�
�����Ѷȣ���