微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一定温度下,将等物质的量A和B充入一密闭容器中,发生如下反应:A(g)+2B(g)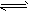 2C(g),反应达到平衡时,若A和B的物质的量之和与C相等,则此时A的转化率为
2C(g),反应达到平衡时,若A和B的物质的量之和与C相等,则此时A的转化率为
[? ]
A.50%
B.60%
C.40%
D.70%
参考答案:C
本题解析:
本题难度:一般
2、选择题 已建立平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列叙述正确的是(? )
①生成物的体积分数一定增加?②生成物的产量一定增加?③反应物的转化率一定增加?④反应物的浓度一定降低?⑤正反应速率一定大于逆反应速率
A.①②④⑤
B.①②③⑤
C.②③
D.②⑤
参考答案:D
本题解析:题中给定了平衡的移动方向,要求判断引起平衡移动的原因及可能产生的结果。平衡向正方向移动,由于改变条件不明,反应物的转化率、浓度均无法确定,则应具体分析使平衡发生移动的原因。若是通过改变温度或改变压强使平衡发生移动,①③④所述情况是成立的;若是通过增加反应物的浓度使平衡向正方向移动,若增加反应物的量很多,生成物体积分数必然降低(混合气体的总物质的量增加),该反应物的浓度较原浓度增大(增加部分较原转化的浓度要少),该物质的转化率较低,故①③④均不确定。由于反应向正方向移动,生成更多的生成物,生成物的量必然增加,故②正确;平衡向正方向移动,必是正反应速率大于逆反应速率的结果,故⑤正确。
本题难度:简单
3、选择题 已知298 K时,2SO2(g)+O2(g)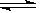 2SO3(g)?ΔH="-197" kJ・mol-1。在同一温度和压强下,向某密闭容器中通入2 mol SO2和1 mol O2达到平衡时,反应放出的热量为Q1,向另一相同的密闭容器中通入1 mol SO2和0.5 mol O2,达到平衡时放出的热量为Q2。下列关系正确的是
2SO3(g)?ΔH="-197" kJ・mol-1。在同一温度和压强下,向某密闭容器中通入2 mol SO2和1 mol O2达到平衡时,反应放出的热量为Q1,向另一相同的密闭容器中通入1 mol SO2和0.5 mol O2,达到平衡时放出的热量为Q2。下列关系正确的是 (?)
(?)
A.Q2=
B.Q2< ="197" kJ
="197" kJ
C.Q2<Q1<197 kJ
D.Q1=Q2="197" kJ
参考答案:C
本题解析:略
本题难度:简单
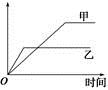
4、选择题 下列表格中的各种情况,可以用如图所示曲线表示的是
选项
| 反应
| 纵坐标
| 甲
| 乙
|
A
| 相同质量的氨气,在同一容器中发生反应:2NH3 N2+3H2 N2+3H2
| 氨气的转化率
| 500 ℃
| 400 ℃
|
B
| 等质量的钾、钠分别与足量的水反应
| H2的质量
| 钠
| 钾
|
C
| 在体积可变的恒压容器中,体积之比为1∶3的N2、H2:N2+3H2 2NH3 2NH3
| 氨气的浓度
| 活性高的催化剂
| 活性一般的催化剂
|
D
| 2 mol SO2和1 mol O2在相同温度下发生反应:2SO2+O2 2SO3 2SO3
| SO3的物质的量
| 2个大气压
| 10个大气压
|
?
参考答案:B
本题解析:温度升高,反应速率加快,达到平衡的时间较短,A项不符合;钾比钠活泼,反应结束的时间较短,等质量的钠、钾与足量水反应产生H2的质量:钠大于钾,B项符合;使用催化剂不能使平衡移动,C项不符合;压强增大,平衡正向移动,SO3的物质的量增大,D项不符合。
本题难度:一般
5、填空题 (16分)现有反应:mA(g)+nB(g)?pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为?热反应,且m+n?p(填“>”、“=”“<”)。
(2)减压时,A的质量分数?(填“增大”“减小”或“不变”)。
(3)若加入B(体积不变 ),则A的转化率?(填“增大”“减小”或“不变”)。
),则A的转化率?(填“增大”“减小”或“不变”)。
(4)若升高温度,则平衡时B、C的浓度之比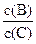 将?(填“增大”“减小”或“不变”)。
将?(填“增大”“减小”或“不变”)。
(5)若加入催化剂,平衡时气体混合物的总物质的量?(填“增大”“减小”或“不变”)。
(6)若B是有色物质,A、 C均无色,则加入C(体积不变)时混合物颜色?(填“变深”、“变浅”或“不变”);而维持容器内压强不变,充入氖气时,混合物颜色?(填“变深”、“变浅”或“不变”)。
参考答案:(16分)
(1)放热?,>?(2)增大?(3)增大
(4)减小?(5)不变?( 6)变深,变浅
6)变深,变浅
本题解析:略
本题难度:一般