微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 实验室用Na2SO4?10H2O配制0.1mol/L的Na2SO4溶液500ml.有以下仪器:
①药匙?②100ml量筒?③1000ml容量瓶?④锥形瓶?⑤玻璃棒?⑥烧杯
(1)配制时,必须选用的仪器为:______(填代号),还缺少的玻璃仪器为______
(2)经计算,本实验需称量硫酸钠晶体(Na2SO4?10H2O)为______g.
(3)用Na2SO4?10H2O配制标准溶液的正确顺序是______.
A.冷却?B.称量?C.洗涤?D.定容?E.溶解?F.摇匀?G.移液
(4)将所配制的Na2SO4溶液进行测定,发现浓度大于0.1mol/L.请你分析配制过程中可能引起该误差的原因是(填字母代号)______
①容量瓶不干燥,含有少量蒸馏水?②定容时俯视刻度线?③定容时仰视刻度线?④未冷却至室温就转移到容量瓶中?⑤没有洗涤烧杯和玻璃棒.
2、选择题 以下是某同学配置250mL?0.2mol/L的NaOH溶液的一些步骤,其中没有错误的是( )
A.在托盘天平的两托盘中分别放等质量的纸,称取2.0gNaOH固体
B.将NaOH固体在烧杯中溶解后迅速小心转移至250mL容量瓶中
C.定容时不小心加水超过了刻度线,此时迅速用胶头滴管吸出一些
D.溶液配置完毕,立即将其转移至带橡胶塞的试剂瓶,贴上标签并洗涤容量瓶
3、选择题 在只含有Na+、Al3+、Cl-、SO42-?四种离子的溶液中(不考虑H+、OH-),已知Na+,Al3+,SO42-的物质的量浓度分别为0.2mol/L,0.1mol/L,0.1mol/L,则溶液中?Cl-的物质的量浓度为( )
A.0.1?mol/L
B.0.2?mol/L
C.0.3?mol/L
D.0.4?mol/L
4、选择题 配制0.1 mol/L的NaCl溶液,下列操作会导致所配溶液浓度偏高的是
[? ]
A.称量时,左盘高,右盘低
B.定容时俯视读取刻度
C.容量瓶洗净后未干燥
D.定容时液面超过了刻度线
5、选择题 李敏同学欲配制250?mL?1.0?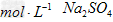 溶液,正确的方法是
溶液,正确的方法是
[? ]
①将35.5?g?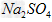 固体溶于250?mL水中?
固体溶于250?mL水中?
②将80.5?g?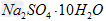 固体溶于少量水中.再用水稀释至250?mL?
固体溶于少量水中.再用水稀释至250?mL?
③将50?mL?5.0?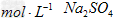 溶液用水稀释至250?mL?
溶液用水稀释至250?mL?
A.①②
B.②③
C.①③
D.①②③?