��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ͼ��ʾ����������ʢ�к�ˮ���������б���ʴʱ���ɿ쵽����˳����
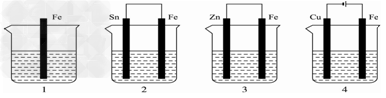
A.4>2>1>3 ������
B.2>1>3>4?����������
C.4>2>3>1 ����
D.3>2>4>1?
�ο��𰸣�A
���������
�����Ѷȣ���
2������� ��ͼ��aΪ������A�ձ��з��뱽��B�ձ���Ϊ1 mol��L��1��ϡ���ᣬC�ձ���Ϊ��ˮ��
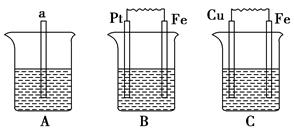
(1)B��Pt���ĵ缫��ӦʽΪ________��
(2)C��Cu���ĵ缫��ӦʽΪ________��Cu��������Һ��pH________(���������С�����䡱)��
(3)�Ƚ�A��B��C��������ʴ�����ʣ��ɿ쵽����˳����________��
(4)ҪʹB�е����ѱ���ʴ���ɽ�B�е�ϡ�����Ϊ________��
�ο��𰸣�(1)2H����2e��=H2��
(2)2H2O��O2��4e��=4OH��������
(3)B>C>A
(4)�ƾ�(�����Ȼ�̼��)
���������(1)B��Pt���ĵ缫��ӦʽΪ2H����2e��=H2����(2)C��Cu����������������ԭ��Ӧ���缫��ӦʽΪ2H2O��O2��4e��=4OH����Cu��������Һ��pH����(3)����Fe��Pt�Ļ�Բ���Fe��Cu��B�з�Ӧ���ʿ죬��A�������DZ��������ױ���ʴ���ʸ�ʴ�����ɿ쵽����˳����B>C>A��(4)ҪʹB�е����ѱ���ʴ���ɽ�B�е�ϡ�����Ϊ�ǵ������Һ����ƾ����������Ȼ�̼�ȡ�
�����Ѷȣ�һ��
3��ѡ���� ��3�֣���2012?ɽ���������������ʴ�йص�˵����ȷ���ǣ�������
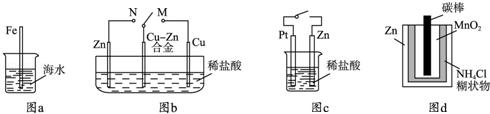
A��ͼa�У����뺣ˮ�е�������Խ�����˸�ʴԽ����
B��ͼb�У�������M������Nʱ��Cu��Zn�Ͻ�ĸ�ʴ���ʼ�С
C��ͼc�У���ͨ����ʱZn��ʴ��������Zn�Ϸų����������Ҳ����
D��ͼd�У�Zn��MnO2�ɵ���Էŵ縯ʴ��Ҫ����MnO2���������������
�ο��𰸣�B
���������A������Һ������Ũ��Խ��ʱ�绯ѧ��ʴԽ���أ�
B��������M������Nʱ��ZnΪ�������Ͻ𱻱�����
C��������Pt�Ϸų���
D��MnO2������ԭ��Ӧ��
�⣺A��ͼa�У�����������ѧ��ʴ�������˵IJ����������Ӵ��٣���ʴ�̶Ƚ��ᣬ��A����
B��ͼb�п�����M����N��Cu��Zn����������ʴ���ʼ�С����B��ȷ��
C��ͼc�н�ͨ����ʱZn����������ʴ��������������Pt�Ϸų�����C����
D��ͼd�иɵ�طŵ�ʱMnO2������ԭ��Ӧ������п�Ļ�ԭ�ԣ���D����
��ѡB��
���������⿼������ĸ�ʴ����������Ŀ�ѶȲ���ע�����ԭ��صĹ���ԭ����
�����Ѷȣ�һ��
4������� ��16�֣�2006����������ӵ���ܲ�������25��ֻ��﮵���������Բ��������Ľ�����Դ���������൱��ģ������������Դ��Ϊ��Ҫ���⡣ij�о�С���ij�Ͼ�����ӵ����������(ͼ�м�Ʒ��ϣ��ɷ�ΪLiMn2O4��ʯī�ۺ�����)���л����о��������������£�

��֪��Li2SO4��LiOH��Li2CO3��303K�µ��ܽ�ȷֱ�Ϊ34.2g��12.7g��1.3g��
��1����������NaOH��Һ��ȡ֮ǰ��Ҫ���з����������Ŀ����?��
��2���Ͼɵ�ؿ������ڷŵ粻��ȫ��������﮵��ʣ�Ϊ�˰�ȫ�Բ�����Ҫ��______?__?��
��3��д����Ӧ�����ɳ���X�����ӷ���ʽ��
?��
��4����֪LiMn2O4��Mn�Ļ��ϼ�Ϊ+3��+4�ۣ�д����Ӧ�ڵ����ӷ�Ӧ����ʽ��
?��
��5������Li2CO3�Ļ�ѧ��Ӧ����ʽΪ______?__����֪Li2CO3��ˮ�е��ܽ�������¶����߶���С�����һ������ʱӦ_?_��
�ο��𰸣���1������Ӵ�������ӿ췴Ӧ���ʣ�2�֣�
��2������������ˮ�֣�2�֣�
(3)CO2+AlO2�C+2H2O=Al(OH)3��+HCO3�C��3�֣�
(4)4 LiMn2O4+4 H++O2=8MnO2+4 Li++2H2O��4�֣�
(5) Li2SO4+Na2CO3��Na2SO4+Li2CO3�� ��3�֣�?���ȹ��ˣ�2�֣�
�����������1�����з��������������Ӧ��ĽӴ�������ӿ췴Ӧ���ʡ�
��2����ǻ��õĽ���������ˮ��������Ӧ��������Ҫ����������ˮ�֡�
��3����Һ�к���ƫ�����ƣ�����ͨ��CO2������������������������ʽΪCO2+AlO2�C+2H2O=Al(OH)3��+HCO3�C��
��4��LiMn2O4��Mn�Ļ��ϼ�Ϊ+3��+4�ۣ���+3�۵ı��������ɶ������̣�����ʽΪ4 LiMn2O4+4 H++O2=8MnO2+4 Li++2H2O��
��5��Li2CO3���ܽ��С������﮵ģ��������﮺�̼���Ʒ�Ӧ��������̼��﮳��������Է���ʽΪLi2SO4+Na2CO3��Na2SO4+Li2CO3��������Li2CO3��ˮ�е��ܽ�������¶����߶���С�����һ������ʱӦ���ȹ��ˡ�
�����Ѷȣ�һ��
5��ѡ���� ���й��ڽ�����ʴ��ȷ����
[? ]
A�������ڳ�ʪ�Ŀ����и�ʴ��ʵ���ǣ�M+nH2O==M(OH)n+n/2H2��
B�������Ļ�ѧ��ʴ��ʵ���ǣ�M-ne-��Mn+������ֱ��ת�Ƹ�������
C�������Ļ�ѧ��ʴ���������������½���
D���ڳ�ʪ�����Ի����У������ĵ绯ѧ��ʴ��Ҫ��������������Ϊ��
�ο��𰸣�BD
���������
�����Ѷȣ���