微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (1)38 g某二价金属氯化物(ACl2)中含有0.8mol Cl-,则ACl2的摩尔质量是________;A的相对原子质量是____________;ACl2的化学式是__________。
(2)质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水。得到的溶液每亳升质量为q g,物质的量浓度为c。则溶质的相对分子质量为 。
参考答案:(1)95g/mol 24 MgCl2;(2)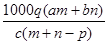
本题解析:(1)38 g某二价金属氯化物(ACl2)中含有0.8mol Cl-,则该物质的物质的量是0.4mol,所以该物质的摩尔质量是38 g÷0.4mol=95g/mol.由于Cl的相对原子质量是35. 5,所以A的相对原子质量是95-35. 5×2=24;相对原子质量是24 的+2价的金属是Mg,所以ACl2的化学式是MgCl2;(2)混合溶液中溶质的质量是m(溶质)=(am+bn)g;蒸发p g水后溶液的质量是m(溶液)=(m+n-p)g,溶液中溶质的质量分数是ω=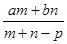 ,溶液的物质的量浓度与溶液的质量分数的关系式是c=
,溶液的物质的量浓度与溶液的质量分数的关系式是c=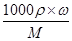 ,所以该物质的摩尔质量是M=
,所以该物质的摩尔质量是M=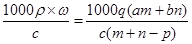 ,而物质的摩尔质量当以g/mol为单位时与相对分子质量相等,所以溶质的相对分子质量为
,而物质的摩尔质量当以g/mol为单位时与相对分子质量相等,所以溶质的相对分子质量为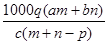 。
。
考点:考查物质与组成微粒的关系、物质的量浓度与质量分数的换算及与物质的相对分子质量的关系。
本题难度:一般
2、选择题 设NA表示阿伏加德罗常数的数值,下列说法正确的是(? )
A.常温常压下,16 g氧气和臭氧的混合物中含有NA个氧原子
B.标准状况下,11.2 L H2O中含分子数为0.5NA
C.标准状况下,22.4 L H2中含质子数为NA
D.100 mL 0.1 mol・L-1的AlCl3溶液中Al3+的个数为0.01NA
参考答案:A
本题解析:设O2的质量为xg,则氧原子个数为(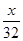 ×2+
×2+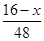 ×3)NA=NA,A对;标准状况下H2O为液体,11.2 L H2O的物质的量不为0.5NA,B错;标准状况下,22.4 L H2中含质子数为2NA,C错;由于Al3+的水解,100 mL 0.1 mol・L-1的AlCl3溶液中Al3+个数小于0.01NA,D错。
×3)NA=NA,A对;标准状况下H2O为液体,11.2 L H2O的物质的量不为0.5NA,B错;标准状况下,22.4 L H2中含质子数为2NA,C错;由于Al3+的水解,100 mL 0.1 mol・L-1的AlCl3溶液中Al3+个数小于0.01NA,D错。
本题难度:一般
3、选择题 设NA为阿附加德罗常数,下列说法正确的是
A.1mol任何氢原子的质量都为1g
B.1.8g铝在化学反应中失去电子数0.2NA
C.28g硅含有6.02×1023个电子
D.1.9g H3O+的质子数为NA
参考答案:B
本题解析:氢有三种,不一定质量都为1。1.8g铝为0.2/3mol,在化学反应中失去电子数0.2mol.
28g硅为1mol约含有6.02×1023×14个电子。1.9g H3O+的物质的量为0.1mol质子数为1.1NA
本题难度:一般
4、选择题 某混合盐溶液中含有0.2 mol Na+、0.25 mol Mg2+、0.4 mol Cl-和x mol SO42-,则x为
A.0.1
B.0.3
C.0.5
D.0.15
参考答案:D
本题解析:由于溶液是电中性的,即0.2mol+0.25mol×2=0.4mol+2x,解得x=0.15mol,答案选D。
本题难度:一般
5、实验题 实验室用氯化钠固体配制1.00 mol/L的NaCl溶液0.5 L,回答下列问题。
(1)请写出该实验的实验步骤:①____,②____, ③____,④____, ⑤____。
(2)所需仪器为:容量瓶(规格:____)、托盘天平、还需要哪些实验仪器才能完成该实验,请写出:
__________________。
(3)试分析下列操作对所配溶液的浓度有何影响及造成该影响的原因。
①为加速固体溶解,可稍微加热并不断搅拌。在未冷却至室温时,将溶液转移至容量瓶定容。对所配溶液浓度的影响:____(填“偏高”、“偏低”或“不影响”),原因是______________________。
②定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响:
____,原因是_________________。
参考答案:
(1)①计算;②称量;③溶解;④转移;⑤定容
(2)500mL;药匙、烧杯、玻璃棒、量筒、胶头滴管
(3)①偏高;未冷却至室温,液体体积膨胀;②偏低;已经定容,再加水相当于稀释了溶液
本题解析:
本题难度:一般