微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如表所示。
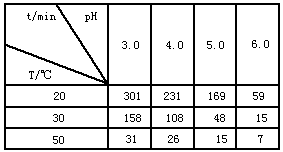
已知:O3的起始浓度为0.021 6 mol/L。
(1)pH增大能加速O3分解,表明对O3 分解起催化作用的是____。
(2)在30℃、pH=4.0条件下,O3的分解速率为____ mol/(L・min)。
(3)据表中的递变规律,推测O3在下列条件下分解速率依次增大的顺序为 ____。(填字母代号)
a. 40℃、pH=3.0
b.10℃、pH=4.0
c.30℃、pH=7.0
参考答案:(1)OH-
(2) 1.00×10-4
( 3)b.a.c
本题解析:
本题难度:一般
2、选择题 镁条和盐酸反应迅速产生大量的氢气,欲使反应速率减慢,可采取的措施有:
①降温;②把镁条粉碎;③加入蒸馏水使盐酸变稀;④升温
A.①②
B.②③
C.①③
D.②④
参考答案:C
本题解析:对于镁和盐酸的反应,可增大浓度、升高温度、增大固体的表面积,或形成原电池反应,可增大反应速率,反之反应速率降低,以此解答该题。①降温,活化分子百分数减小,反应速率减小,故正确;②把镁条粉碎,固体表面积增大,反应速率增大,故错误;③加入蒸馏水使盐酸变稀,浓度减小,反应速率减小,故正确;④升温,活化分子百分数增大,反应速率增大,故错误,故选C。
本题难度:简单
3、实验题 (10分)某研究小组为了研究不同条件下金属铝粉在过量稀硫酸中的溶解性能,设计如下实验。已知:c(H2SO4)="4.5" mol・L-1,反应均需要搅拌60min。
编号
| 温度/℃
| 加入某盐
| H2SO4体积/mL
| H2O体积/mL
| 铝粉加入量/g
| 铝粉溶解量 /g
|
①
| 20
| 不加
| 40
| 0
| 2.0050
| 0.0307
|
②
| 80
| 不加
| 40
| 0
| 2.0050
| 0.1184
|
③
| t1
| 不加
| 20
| V1
| 2.0050
|
|
参考答案:
本题解析:
本题难度:困难
4、选择题 下列相关实验不能表达预期目的是( )
| 相关实验 | 预期目的
A
把等质量的两份同种大理石块中的一份研成粉末,在同温度下分别与等体积同浓度的盐酸反应,观察放出气体快慢
验证接触面积对化学反应速率的影响
B
把装有颜色相同的NO2与N2O4混合气体的小试管(密封)分别浸入热水和冷水中,观察试管中气体颜色变化
验证温度对化学平衡的影响
C
在蔗糖中加入适量的硫酸溶液,加热,充分水解后加入新制的氢氧化铜悬浊液并加热,观察沉淀的颜色
验证蔗糖水解产物中有醛基的存在
D
在装有同样浑浊的苯酚溶液的两个试管中,对其中一支试管加热,观察溶液是否变澄清
比较苯酚在不同温度下的溶解度
|
A.A
B.B
C.C
D.D
参考答案:A.相同温度下,等质量的大理石块、大理石粉分别与等体积、等浓度的盐酸反应,大理石与盐酸反应的接触面积不同,反应速率不同,能达到目的,故A不选;
B.升高温度,导致二氧化氮和四氧化二氮之间的平衡改变而向吸热方向移动,能达到目的,故B不选;
C.在蔗糖中加入稀硫酸,水浴加热,溶液呈酸性,葡萄糖和氢氧化铜的反应必须在碱性条件下反应,不能达到目的,故C选;
D.苯酚加热后溶解度增大,在冷水和热水中的溶解度不同,能达到实验目的,故D不选.
故选C.
本题解析:
本题难度:一般
5、填空题 (10分)臭氧是一种强氧化剂,常用于消毒、灭菌等。
(1)O3与KI溶液反应生成的两种单质是 和 (填分子式)。
(2)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如表所示。已知:O3的起始浓度为 0.021 6 mol/L。
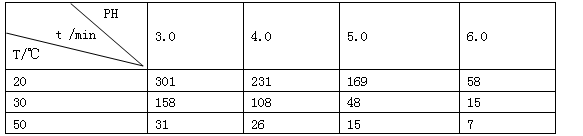
①pH增大能加速O3分解,表明对O3分解起催化作用的是 。
②在30℃、pH=4.0条件下,O3的分解速率为 。
③据表中的递变规律,推测O3在下列条件下分解速率依次增大的顺序为 (填字母代号)。
A.40 ℃、pH=3.0 B.10 ℃、pH=4.0 C.30 ℃、pH=7.0
参考答案:(1)O2、I2;
(2)①OH-;②1.00×10-4mol/(L・min);
③b<a<c;
本题解析:(1)O3与KI溶液反应不可能生成K单质,故生成的两种单质只能为O2、I2。
(2)①由表中数据可知:pH由3.0到6.0增大,O3分解速率加快,则OH-浓度增大,化学反应速率加快,所以表明OH-对O3分解起催化作用;
②在30℃、pH=4.0条件下,O3的分解速率为:v=△c/△t=0.0108mol/L=1.00×10-4mol/(L・min);
③由表中数据可知,40°C、pH=3.0时,所需时间t1:31min<t1<158min之间;10°C、pH=4.0时,所需时间t2>231min;30°C、pH=7.0时,所需时间t3<15min,则分解速率依次增大的顺序为b<a<c;
考点:了解化学反应速率的概念、反应速率的定量表示方法。理解外界条件(浓度、温度、压强、催化剂等)对反应速率的影响,认识并能用相关理论解释其一般规律。
点评:考查影响速率的因素,培养学生分析利用实验数据的能力。
本题难度:一般