微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在密闭容器中发生下列反应aA(g)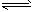 cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
[? ]
A.A的转化率变小
B.平衡向正反应方向移动
C.D的体积分数变大
D.a > c+d
参考答案:A
本题解析:
本题难度:一般
2、选择题 已建立化学平衡的某可逆反应,当改变反应条件使化学平衡向正反应方向移动时,下列叙述正确的是
[? ]
①生成物的体积分数一定增加 ②生成物的产量一定增加
③反应物的转化率一定增大 ④反应物的浓度一定降低
⑤正反应速率一定大于逆反应速率 ⑥使用了合适的催化剂
A.①②
B.②⑤
C.③⑤
D.④⑥
参考答案:B
本题解析:
本题难度:一般
3、选择题 下列事实,不能用勒夏特列原理解释的是( )
A.溴水中有下列平衡Br2+H2O?HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
B.对2HI(g)?H2(g)+I2(g),平衡体系增大压强可使颜色变深
C.反应CO+NO2?CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
D.合成NH3反应为放热反应,为提高NH3的产率,理论上应采取低温度的措施
参考答案:A、溴水中加入AgNO3溶液后,生成溴化银沉淀,溴离子浓度降低,使得化学平衡Br2+H2O?HBr+HBrO向右移动,能用勒夏特列原理解释,故A不符合;
B、该反应反应前后气体体积不变,所以压强不影响化学平衡的移动,增大平衡体系的压强气体的体积减小,碘的浓度增大,颜色变深,所以不能用勒夏特列原理解释,故B符合;
C、该反应正反应是放热反应,升高温度,平衡向逆反应方向移动,能用勒夏特列原理解释,故C不符合;
D、合成氨的正反应是放热反应,降低温度平衡向逆反应方向移动,为提高NH3的产率,理论上应采取低温度的措施,所以能用勒夏特列原理解释,故D不符合;
故选B.
本题解析:
本题难度:简单
4、选择题 现有如下四个图象下列反应中全部符合上述图象的反应是

[? ]
A.N2(g)+3H2(g)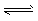 2NH3(g)ΔH=-Q1 kJ/mol(Q1>0)
2NH3(g)ΔH=-Q1 kJ/mol(Q1>0)
B.H2(g)+CO(g)  C(s)+H2O(g)ΔH=+Q4 kJ/mol(Q4>0)
C(s)+H2O(g)ΔH=+Q4 kJ/mol(Q4>0)
C.4NH3(g)+5O2(g)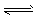 4NO(g)+6H2O(g)ΔH=-Q3 kJ/mol(Q3>0)
4NO(g)+6H2O(g)ΔH=-Q3 kJ/mol(Q3>0)
D.2SO3(g)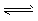 2SO2(g)+O2(g)ΔH=+Q2 kJ/mol(Q2>0)
2SO2(g)+O2(g)ΔH=+Q2 kJ/mol(Q2>0)
参考答案:D
本题解析:
本题难度:一般
5、选择题 Cl2通入水中发生如下反应:Cl2+H2O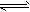 HCl+HClO,欲增大所得溶液中HClO的浓度,应采取的措施为
HCl+HClO,欲增大所得溶液中HClO的浓度,应采取的措施为
[? ]
A.加Na2CO3固体
B.加NaOH固体
C.加水
D.通入NH3气
参考答案:A
本题解析:
本题难度:一般