微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 CO与H2在催化剂作用下合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g).在容积均为1L的a、b、c、d、e五个密闭容器中分别充入等量的1mol?CO和2mol?H2混合气体,控温.实验测得相关数据如下图1和图2.
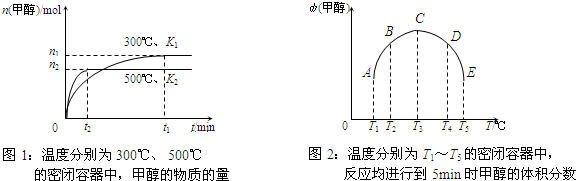
下列有关说法正确的是( )
A.该反应的正反应是气体体积减小的吸热反应
B.K1<K2(K为该条件下反应的平衡常数)
C.反应进行到5min时,a、b两容器中平衡正向移动,d、e两容器中平衡逆向移动
D.将容器c中的平衡状态转变到容器d中的平衡状态,可采取的措施有升温或减压
2、选择题 反应2A(g)?2B(g)+E(g)△H>0,达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是( )
A.加压
B.减压
C.减小E的浓度
D.降温
3、选择题 采用以下措施一定会使一个平衡体系发生移动的是( )
A.加入一种反应物
B.对平衡体系增加压强
C.改变温度
D.使用催化剂
4、填空题 在稀氨水中存在平衡:NH3+H2O NH4++OH-,如进行下列操作,则NH3、NH4+、H+、OH-浓度如何变化?试用“增大”“减小”“不变”填写。
NH4++OH-,如进行下列操作,则NH3、NH4+、H+、OH-浓度如何变化?试用“增大”“减小”“不变”填写。
(1)通适量HCl气体时,c(NH3)________,c(H+)____________。
(2)加入少量NaOH固体时,c(NH4+)________,c(OH-)________。?
(3)加入NH4Cl晶体时,c(NH4+)________,c(OH-)________。
5、填空题 (1)某温度下体积为100 L的氨合成塔中(已知合成氨的反应为放热反应),测得各物质浓度(mol/L)的变化如表:根据表中数据计算0~2h 内N2的平均反应速率为__________。请用下表中适当的数据表示该反应的平衡常数表达式:______________。

(2)反应在4-5h之间,平衡向正方向移动,可能的原因是_________。(选填A~ F,下同)表中5-6h之间数值发生变化,可能的原因是________。
A.移走了氨气 B.降低温度 C.加压 D.增加氢气浓度 E.升高温度 F.增加氮气浓度
(3)将NH3通入到0.04 mol/L的FeCl3溶液中,要使溶液中Fe3+沉淀较完全(即Fe3+浓度降至原来的千分之一),则溶液的pH为_______[已知常温下,Fe(OH)3的溶度积常数Ksp=4×10-38]