微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
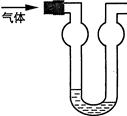
1、选择题 双球洗气管是一种多用途仪器,常用于去除杂质、气体干燥、气体吸收(能防止倒吸)等实验操作。右图是用水吸收下列某气体时的情形,根据下面附表判断由左方进入的被吸收气体是?
A.Cl2
B.HCl
C.H2S
D.CO2
参考答案:B
本题解析:四种气体的溶解度表(室温下)
附:
气体
Cl2
HCl
H2S
CO2
l体积水约能吸收气体体积数
2
500
2.6
1
?
由四种气体的溶解度表可以看出,HCl溶解度最大,溶解的速率大于气体进入洗气管的速率,导致左侧洗气管气压降低,出现如图所示情形。
本题难度:一般
2、填空题 (每空1分,共5分).可用于分离或提纯物质的方法有:①过滤②蒸馏③加热④分液(填序号)
(1)除去石灰水中悬浮的CaCO3颗粒?
(2)除去NaCl晶体中混有的碘单质?
(3)分离石油中各不同沸点范围的成分?
(4)分离水和苯的混合物?
(5)分离CCl4(沸点76.75℃)和甲苯(沸点110.6℃)____________。
参考答案:(1)①? (2)③? (3)②? (4)④? (5)②
本题解析:(1)过滤适用于不溶性固体和液体之间的一种分离方法,碳酸钙不溶于水,过滤即可,答案选①。
(2)碘易升华,所以除去氯化钠晶体中的单质碘加热即可,答案选③。
(3)蒸馏是依据混合物中个组分沸点不同而分离的一种法,适用于除去易挥发、难挥发或不挥发杂质,所以答案选②。
(4)分液适用于互不相溶的液体之间的一种分离方法,苯不溶于水,分液即可,答案选④。
(5)四氯化碳和甲苯的沸点相差较大,蒸馏即可,答案选②。
本题难度:简单
3、选择题 在NaCl、MgCl2、MgSO4形成的混合溶液中,c(Na+)=0.10mol?L-1,c(Mg2+)=0.25mol?L-1,c(Cl-)=0.20mol?L-1,则c(SO42-)为
A.0.15mol?L-1
B.0.10mol?L-1
C.0.25mol?L-1
D.0.20mol?L-1
参考答案:D
本题解析:分析:令硫酸根的物质的量浓度为c,根据溶液中阴阳离子所带的正负电荷总数相等,列式计算c值.据此判断.
解答:令硫酸根的物质的量浓度为c,根据溶液中阴阳离子所带的正负电荷总数相等,则:
0.10mol?L-1×1+0.25mol?L-1×2=0.20mol?L-1×1+2c
解得:c=0.2mol/L.
故选:D.
点评:考查溶液物质的量浓度的计算,难度不大,利用常规解法,比较麻烦,本题根据溶液不显电性阳离子与阴离子所带电荷总数相等,即电荷守恒原则解答,注意电荷守恒原则在混合溶液有关离子浓度计算经常运用.
本题难度:一般
4、选择题 下列实验原理及操作中,正确的是.
A.用酒精做萃取剂萃取碘水中的碘单质
B.配制1.00mol?L-1Na2CO3溶液时,将称好的Na2CO3固体直接放入容量瓶中溶解
C.向某溶液中滴加BaCl2溶液,有白色沉淀,再滴加足量稀HCl,若沉淀不溶解,则说明原溶液中一定含SO42-
D.在某试样中加入NaOH溶液,加热,产生能使湿润的红色石蕊试液变蓝的气体即证明试样中含有NH4+
参考答案:D
本题解析:
本题难度:一般
5、填空题 综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如下图所示:

(1)反应①~⑤中,属于氧化还原反应的是?(填编号)。
(2)写出反应②的离子方程式?。
(3)X溶液中的主要阳离子是Na+和?。
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:
①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③?;④加适量盐酸;⑤?。(请补全缺少的实验步骤)
(5)检验纯碱样品中是否含NaCl应选用的试剂是?。
参考答案:(1)⑤?(2分)?
(2)Mg (OH)2+2H+ = Mg2+ + H2O (2分)
(3)NH4+(2分)
(4)过滤 (2分) 、蒸发结晶(其它答案合理也给分)(2分)?
(5)稀硝酸、AgNO3溶液(2分)
本题解析:(1)反应①②属于复分解反应,③属于化合反应,④属于分解反应,⑤为氧化还原反应;(2)酸碱中和反应,Mg (OH)2不溶于水写成化学式,Mg (OH)2+2H+ = Mg2+ + H2O;(3)该反应为氨水、二氧化碳、氯化钠反应生成碳酸氢钠沉淀和氯化铵,X溶液中的主要阳离子是NH4+和Na+;(4)加入盐酸前生成的沉淀能溶解于盐酸,故应过滤除去沉淀后再加盐酸,然后通过蒸发结晶得到氯化钠晶体;(5)检验样品中是否含有氯离子,用硝酸酸化的硝酸银。
本题难度:一般