��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��2L�ܱ����������2mol M��һ������N���������·�Ӧ��M(g)+N(g)  ?E(g)������Ӧ���е�4minʱ����֪M��Ũ��Ϊ0��2mol/L����Ӧ���е�2minʱ���ܱ�������M�����ʵ���Ũ��Ϊ?��?��
?E(g)������Ӧ���е�4minʱ����֪M��Ũ��Ϊ0��2mol/L����Ӧ���е�2minʱ���ܱ�������M�����ʵ���Ũ��Ϊ?��?��
A������0��6mo l/L
l/L
B����0��6mol/L
C������0��8mol/L
D������0��8mol/L
�ο��𰸣�B
�����������
�����Ѷȣ���
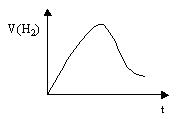
2��ʵ���� ��ZnͶ��һ��Ũ��һ������������У�H2������������ʱ��Ĺ�ϵ��ͼ��ʾ���Խ���ͼ�����߱仯��ԭ��������ΪH2���������ʣ�������Ϊʱ�䣩��
�𣺢� ��
�� ��
�ο��𰸣��ٷ�Ӧ��ʼʱ����Ӧ���ȣ���Ӧ���ʽϿ죻�����ŷ�Ӧ�Ľ��У�HCl���ʵ���Ũ�ȱ�С����Ӧ�����ֱ���.
��������������������ΪC��Zn�����ᷴӦ�Ƿ��ȷ�Ӧ���÷�Ӧ��Ӱ�컯ѧ��Ӧ���ʵ�������������һ�Ƿ�Ӧ�ų�������ʹ��Ӧ���������Ƿ�ӦʹHCl���ʵ���Ũ�ȼ�С����Ӧ���ʼ�С����ͼ���֪���ڿ�ʼʱ�¶ȱ仯��Ӱ�췴Ӧ���ʵ���Ҫ����,�����ŷ�Ӧ�Ľ���,HCl���ʵ���Ũ�ȵļ�С��Ӱ�췴Ӧ���ʵ���Ҫ���ء��𰸣��ٷ�Ӧ��ʼʱ����Ӧ���ȣ���Ӧ���ʽϿ죻�����ŷ�Ӧ�Ľ��У�HCl���ʵ���Ũ�ȱ�С����Ӧ�����ֱ���.
ѧ��ָ�������⿼��ͨ��ͼ�����Ӱ�컯ѧ��Ӧ���ʵ����ء�ͼ�����Ӧע�����¼����棺(1)�����(2)���յ�(3)���仯���ƣ����塰���䡱�͡�ͻ�䡱������䡱�͡�С�䡱�ȡ�
�����Ѷȣ���
3��ѡ���� ��C+CO2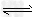 2CO?;?����ӦΪ���� ��Ӧ����Ӧ����ΪV1��N2+3H2
2CO?;?����ӦΪ���� ��Ӧ����Ӧ����ΪV1��N2+3H2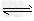 2NH3;?����ӦΪ���ȷ�Ӧ����Ӧ����ΪV2������������Ӧ�����¶�����ʱ��V1��V2�ı仯���Ϊ��
2NH3;?����ӦΪ���ȷ�Ӧ����Ӧ����ΪV2������������Ӧ�����¶�����ʱ��V1��V2�ı仯���Ϊ��
[? ]
A.ͬʱ����? ?
B.ͬʱ���١�
C.V1����V2��С ?
D.V1����V2����
�ο��𰸣�A
���������
�����Ѷȣ���
4��ѡ���� ��2L�ܱ������м���4molA��6molB���������·�Ӧ��4A��g��+6B��g��?4C��g��+5D��g��������5���Ӻ�ʣ�µ�A��2.5mol����B�ķ�Ӧ�����ǣ�������
A��0.45mol/��L?s��
B��0.15mol/��L?s��
C��0.225mol/��L?s��
D��0.9mol/��L?s��
�ο��𰸣�5s��A�����ʵ����仯��Ϊ4mol-2.5mol=1.5mol����A��Ũ�ȱ仯��Ϊ1.5mol2L=0.75mol/L������v��A��=0.75mol/L5s=0.15mol/��L?s��������֮�ȵ��ڻ�ѧ������֮�ȣ�����v��B��=64��0.15mol/��L?s��=0.225mol/��L?s����
��ѡC��
���������
�����Ѷȣ���
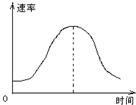
5��ѡ���� ��þ��Ͷ�뵽ʢ������ij������������H2�����ʿ�����ͼ��ʾ�������������У��������Ũ�ȣ���þ���ı����������Һ���¶ȣ���Cl-��Ũ�ȣ�Ӱ�췴Ӧ���ʵ������ǣ�������
A���٢�
B���ۢ�
C���٢ڢ�
D���ڢ�