��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ӦC (s) + H2O (g)  CO(g) + H2 (g)��һ�ɱ��ݻ����ܱ������н��У����������ĸı���䷴Ӧ���ʼ�����Ӱ�����?��?��?
CO(g) + H2 (g)��һ�ɱ��ݻ����ܱ������н��У����������ĸı���䷴Ӧ���ʼ�����Ӱ�����?��?��?
A������C�����ʵ���
B���������������Сһ��
C�����߷�Ӧ���¶�
D������ѹǿ�������N2ʹ����������
�ο��𰸣�A
���������Ӱ�췴Ӧ���ʵ��������һ�����¶ȡ�Ũ�ȡ�ѹǿ�ʹ����ȣ�����̼�ǹ��壬�ı����������Է�Ӧ�����Dz���Ӱ��ģ�����ѡ����B��Cʹ��Ӧ���ʼӿ죬Dʹ��Ӧ���ʽ��ͣ���ѡA��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������ǿ�����ؿ���ѧ�����������Ӱ�췴Ӧ���ʵ���Ϥ�˽����ճ̶ȡ�����Ĺؼ�����ȷŨ�ȶԷ�Ӧ����Ӱ��������Dz��������ڹ����Һ�壬��Ҫ�������⡢���������
�����Ѷȣ���
2��ѡ���� ��Ӧ4NH3������+5O2������?

4NO������+6H2O��������2�����ܱ������н��У�1���Ӻ�NH3������0.12Ħ������ƽ��ÿ����Ũ�ȱ仯��ȷ���ǣ�������
A��NO��0.001Ħ/��
B��H2O��0.002Ħ/��
C��NH3��0.002Ħ/��
D��O2��0.00125Ħ/��
�ο��𰸣���1���Ӻ�NH3������0.12Ħ��������NH3��ʾ�Ļ�ѧ��Ӧ����ΪV��NH3��=��C��t=��n?V?��t?=0.12mol?2L60s=0.001mol?��L?s��-1
A���ɻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���v��NO��=V��NH3��=0.001 mol?��L?s��-1������NOƽ��ÿ����Ũ�ȱ仯Ϊ0.001Ħ/������A��ȷ��
B���ɻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���V��H2O��=64V��NH3��=0.0015 mol?��L?s��-1������NOƽ��ÿ����Ũ�ȱ仯Ϊ0.0015Ħ/������B����
C����V��NH3��=0.001mol?��L?s��-1������NH3ƽ��ÿ����Ũ�ȱ仯Ϊ0.001Ħ/������C����
D���ɻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���V��O2��=54V��NH3���T0.00125 mol?��L?s��-1������O2ƽ��ÿ����Ũ�ȱ仯Ϊ0.00125Ħ/������D��ȷ��
��ѡ��AD��
���������
�����Ѷȣ�һ��
3��ѡ���� һ�������£���Ӧ2SO2��g����O2��g�� 2SO3��g����10L���ܱ������н��У����4min�ڣ�SO2�����ʵ�����20mol��С��4mol���������������䣬SO2��Ũ�ȱ�Ϊ0.8mol/L����Ҫʱ��Ϊ��?��
2SO3��g����10L���ܱ������н��У����4min�ڣ�SO2�����ʵ�����20mol��С��4mol���������������䣬SO2��Ũ�ȱ�Ϊ0.8mol/L����Ҫʱ��Ϊ��?��
A��3min
B����3min
C������3min
D��4min
�ο��𰸣�
���������Bǰ4�����ڣ���������Ũ����2mol/L��Ϊ0.4mol/L����������Ӧ����Ϊ0.4mol/(L��min)����ʹ��������Ũ�ȱ�Ϊ0.8mol/L�����������Ӧ���ʴ���0.4mol/(L��min)������v="1.2/t" mol/(L��min)>0.4 mol/(L��min)��t<3min��
���������ŷ�Ӧ���У���Ӧ���ʼ�С��
�����Ѷȣ�һ��
4������� ��֪A(g)+B(g)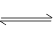 C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
�¶�/��
| 700
| 900
| 830
| 1000
| 1200
|
ƽ�ⳣ��
| 1.7
| 1.1
| 1.0
| 0.6
| 0.4
|
�ش��������⣺
(1)�÷�Ӧ��ƽ�ⳣ������ʽK= ����H 0���<���� >���� =��)��
(2)830��ʱ����һ��5 L���ܱ������г���0.20mol��A��0.80mol��B���練Ӧ��ʼ6s��A��ƽ����Ӧ����v(A)=0��003 mol��L-1��s-1��
��6sʱc(A)= mol��L-1�� C�����ʵ���Ϊ mol��
����Ӧ��һ��ʱ��ﵽƽ��ʱA��ת����Ϊ ��
�����ʱ����ܱ��������ٳ���1 mol�����ƽ��ʱA��ת����Ϊ ��
(3)�жϸ÷�Ӧ�Ƿ�ﵽƽ�������Ϊ (����ȷѡ��ǰ����ĸ)��
a��ѹǿ����ʱ��ı� b.������ܶȲ���ʱ��ı�
c. c(A)����ʱ�ʸı� d.��λʱ��������c��D�����ʵ������
(4)1200��ʱ��ӦC(g)+D(g)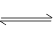 A(g)+B(g)��ƽ�ⳣ����ֵΪ ��
A(g)+B(g)��ƽ�ⳣ����ֵΪ ��
�ο��𰸣���1��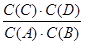 ����2��0.022 0.09 80% 80% ����2�֣�
����2��0.022 0.09 80% 80% ����2�֣�
��3��C ��4��2.5
�����������1�����淴ӦA��g��+B��g��?C��g��+D��g����ƽ�ⳣ������ʽk=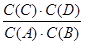 ���ɱ������ݿ�֪���¶�Խ��ƽ�ⳣ��ԽС��˵�������¶�ƽ�����淴Ӧ�ƶ���������Ӧ�Ƿ��ȷ�Ӧ������H��0��
���ɱ������ݿ�֪���¶�Խ��ƽ�ⳣ��ԽС��˵�������¶�ƽ�����淴Ӧ�ƶ���������Ӧ�Ƿ��ȷ�Ӧ������H��0��
��2����Ӧ��ʼ6s��A��ƽ����Ӧ����v��A��=0.003mol?L-1?s-1����6s�ڡ�c��A��=0.003mol?L-1?s-1��6s=0.018mol/L��A����ʼŨ��Ϊ0.20/5=0.04mol/L����6sʱʱc��A��=0.04mol/L-0.018mol/L=0.022mol/L����6s�ڡ�n��A��=0.018mol/L��5L=0.09mol���ɷ���ʽ��֪n��C��=��n��A��=0.09mol����ƽ��ʱA��Ũ�ȱ仯��Ϊx����
A��g��+B��g�� ? C��g��+D��g��
��ʼ��mol/L����0.04 0.16 0 0
�仯��mol/L����x x x x
ƽ�⣨mol/L����0.04-x 0.16-x x x
��x��x/[(0.04-x)��(0.16-x)]=1�����x=0.032
����ƽ��ʱA��ת����Ϊ0.032/0.04��100%=80%��
������䣬����1mol�������Ӧ��������ֵ�Ũ�Ȳ��䣬�仯���ƶ���A��ת���ʲ���Ϊ80%��
��3���÷�Ӧǰ����������ʵ������䣬ѹǿʼ�ղ��䣬��ѹǿ����ʱ��ı䣬����˵������ƽ�⣬��a�������������������䣬�������ݻ����䣬�ʻ��������ܶ�ʼ�ղ��䣬��������ܶȲ���ʱ��ı䣬����˵������ƽ�⣬��b�����淴Ӧ����ƽ��ʱ������ֵ�Ũ�Ȳ������仯����c��A������ʱ��ı䣬˵������ƽ�⣬��c��ȷ����λʱ��������C��D�����ʵ�����ȣ�����ʾ����Ӧ���ʣ���Ӧʼ�հ�1��1����C��D�����ʵ���������˵������ƽ�⣬��d�������Ա���Ĵ�ѡ��c��
��4��ͬһ��Ӧ����ͬ�¶��£������淴Ӧ�����ƽ�ⳣ����Ϊ��������1200��ʱ��Ӧ
C��g��+D��g��?A��g��+B��g����ƽ�ⳣ����ֵΪ1/0.4=2.5
���㣺��ѧƽ����㡢ƽ�ⳣ�����㡢��ѧ��Ӧ���ʡ�ƽ��״̬�ж�
���������⿼�黯ѧƽ����㡢ƽ�ⳣ�����㡢��ѧ��Ӧ���ʡ�ƽ��״̬�жϣ��Ѷ��еȣ�ע�⻯ѧƽ��״̬�жϣ�ѡ���жϵ������������ŷ�Ӧ�Ľ��з����仯�������������ɱ仯����ֵʱ��˵�����淴Ӧ����ƽ��״̬��
�����Ѷȣ�����
5��ѡ���� ����˵������ȷ���ǣ�������
A���ܹ�������Ч��ײ�ķ��ӽ��������
B�������¶ȣ�����Ӱٷ�������ѧ��Ӧ��������
C�����뷴Ӧ�����Ӱٷ�������ѧ��Ӧ��������
D��ʹ�ô���������Ӱٷ�������ѧ��Ӧ��������
�ο��𰸣�A����������ܹ�������Ч��ײ�ķ��ӣ���A��ȷ��
B�������¶ȣ�����Ӱٷ����������Ի�ѧ��Ӧ��������B��ȷ��
C�����뷴Ӧ�����Ӱ�����Ӱٷ�����������������Ч��ײ����ѧ��Ӧ��������C����
D��ʹ�ô���������Ӱٷ�������ѧ��Ӧ��������D��ȷ��
��ѡ��C��
���������
�����Ѷȣ���