微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 人类对某金属冶炼技术的掌握程度决定了其应用的广泛性.影响冶炼方法的主要因素是( )
A.金属的活动性大小
B.金属在地壳中的含量多少
C.金属的化合价高低
D.金属的导电性强弱
参考答案:A
本题解析:
本题难度:一般
2、选择题 工业冶炼钨采取的方法是( )
A.热分解法
B.热还原法
C.电解法
D.自然界存在直接得到
参考答案:B
本题解析:
本题难度:简单
3、简答题 (一)括号中的物质是杂质,写出除去这些杂质的试剂:
(1)MgO?(Al2O3)______(2)Cl2(HCl)______
(3)FeCl3(FeCl2)______(4)NaHCO3溶液(Na2CO3)______
(二)海水中含有大量的氯化镁,从海水中提取镁的生产流程如图1所示:
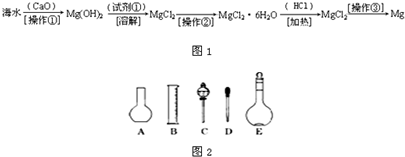
回答下列问题:
写出在海水中加入氧化钙生成氢氧化镁的化学方程式______;
操作①主要是指______;试剂①可选用______;操作②是指______;经操作③最终可得金属镁.
(三)实验室配制480ml?0.1mol?L-1的Na2CO3溶液,回答下列问题:
(1)应用托盘天平称取十水碳酸钠晶体______g.
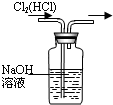
(2)如图2所示的仪器配制溶液肯定不需要的是______(填序号),本实验所需玻璃仪器E规格为______mL.
(3)容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的______.(填数字符号)
(4)配制所需的主要仪器是:a容量瓶、b烧杯、c胶头滴管、d托盘天平,它们在操作过程中使用的前后顺序是______.(填写字母,每种仪器只能选择一次)
(5)玻璃棒是化学实验中常用的一种玻璃工具,则在配制溶液的过程中玻璃棒共起到了______种用途.(填写数字)
(6)若实验时遇到下列情况,将使溶液的浓度偏低的是______.
A.配制前设有将容量瓶中的水除尽;?B.碳酸钠失去了部分结晶水;
C.碳酸钠晶体不纯,其中混有氯化钠;?D.称量碳酸钠晶体时所用砝码生锈;? E.定容时仰视刻度线.
参考答案:(一)(1)MgO?(Al2O3)二者都难溶于水,根据分类和性质MgO是碱性氧化物,具有碱性氧化物的通性,溶于酸而不溶于碱;Al2O3是两性氧化物,具有两性氧化物的通性,溶于强酸强碱.所以可把混合物加入强碱溶液中,Al2O3能和氢氧化钠溶液反应,Al2O3+2OH-=2AIO2-+H2O,然后过滤,可得较纯的MgO,故答案为:NaOH溶液;
(2)Cl2(HCl)氯化氢极易溶于水,氯气能溶于水,且与水反应,Cl2+H2O=H++Cl-+HClO,食盐水溶液中的氯离子抑制氯气的溶解,降低氯气的溶解度,所以可用饱和食盐水除去氯气中混有的氯化氢气体,故答案为:饱和NaCl溶液;
(3)FeCl3(FeCl2) 除去FeCl3溶液中的少量FeCl2,选择氯气或氯水等,发生的离子反应为2Fe2++Cl2=2Fe3++2Cl-,故答案为:氯气或氯水;
(4)NaHCO3溶液(Na2CO3) 除去NaHCO3溶液中含有的Na2CO3溶质可在溶液中通入过量二氧化碳气体,Na2CO3溶液可与二氧化碳反应生成NaHCO3,反应的离子方程式为CO32-+H2O+CO2=2HCO3-,故答案为:CO2;
(二)在海水中加入氧化钙,氧化钙和水反应会生成氢氧化钙,CaO+H2O=Ca(OH)2①,氢氧化钙和氯化镁反应会生成氢氧化镁沉淀和氯化钙,Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2②,总的方程式①+②得:CaO+MgCl2+H2O=Mg(OH)2+CaCl2,氧化钙和水会生成氢氧化钙,氢氧化钙和氯化镁会生成氢氧化镁沉淀,所以操作1的名称是过滤,氢氧化镁沉淀和盐酸反应生成氯化镁和水,Mg(OH)2+2HCl=MgCl2+2H2O,所以试剂①可选用盐酸,由氯化镁溶解度受温度的影响决定通过什么方法使溶质从它的饱和溶液中结晶析出,氯化镁溶解度受温度的影响变化不大,所以操作②的名称是蒸发浓缩,冷却结晶,过滤,电解氯化镁生成金属镁和氯气,该反应的化学方程式:MgCl2?通电?.?Mg+Cl2↑,
故答案为:CaO+MgCl2+H2O=Mg(OH)2+CaCl2;过滤;HCl;蒸发浓缩,冷却结晶,过滤;
(三)(1)没有480mL的容量瓶,应选择大于480mL且规格相近的容量瓶,故选择500mL容量瓶;
配制500mL0.1mol?L-1的Na2CO3溶液需要碳酸钠的质量为:0.1mol?L-1×0.5L=0.05mol,Na2CO3?10H2O的物质的量等于Na2CO3的物质的量,所以Na2CO3?10H2O的质量0.05mol×286g/mol=14.3g;
故答案为:14.3;
(2)配制顺序是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀→装瓶贴签,一般用天平称量(用到药匙)称量,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀.所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,不需要圆底烧瓶,分液漏斗,
故答案为:AC;500ml;
(3)根据容量瓶上标有温度、容量、刻度线,故选:①③⑤;
(4)操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,故在操作过程中使用的前后顺序是:d?b?a?c;
故答案为:d?b?a?c;
(5)溶解是玻璃棒用于搅拌加速溶解,移液时引流作用,故答案为:2;
(6)A.溶液配制需加水定容,配制前没有将容量瓶中的水除尽,容量瓶未经干燥就使用不影响溶质的物质的量,也不影响溶液的体积,所以对配制的溶液浓度无影响,故A错误;
B.碳酸钠失去了部分结晶水,导致称量溶质的质量增大,所以溶质的物质的量偏大,配制溶液的浓度偏高,故B错误;
C.碳酸钠晶体不纯,其中混有氯化钠,导致碳酸钠的物质的量偏小,配制溶液的浓度偏低,故C正确;
D.称量碳酸钠晶体时所用砝码生锈,导致称量溶质的质量增大,所以溶质的物质的量偏大,配制溶液的浓度偏高,故D错误;
E.若定容时仰视刻度线,导致溶液的体积偏大,所以配制溶液的浓度偏低,故E正确;
故选CE.
本题解析:
本题难度:一般
4、选择题 下列装置所示的实验中,能达到实验目的是( )
A.
除去Cl2中的HCl
B.
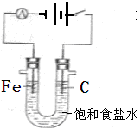
电解制氯气和氢气
C.
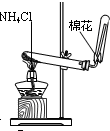
实验室制氨气
D.

分离碘酒中的碘和酒精
参考答案:B
本题解析:
本题难度:简单
5、选择题 用铝热法还原下列物质,制得金属各1mol,消耗铝最少的是( )
A.Fe3O4
B.MnO2
C.Cr2O3
D.V2O5
参考答案:A
本题解析:
本题难度:一般