��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����ѧ�ҳɹ��Ƴ���һ�����͵�̼��������û����ᄃ����ÿ��̼ԭ�Ӿ����ĸ����۵�������ԭ�ӽ��Ϊһ�ֿռ���״��������չ�ṹ�����жԸþ��������������
A���þ���������ԭ�Ӿ���
B��������̼ԭ������C��O��ѧ����֮��Ϊ1��2
C������Ŀռ���С������12��ԭ�ӹ���
D���þ�����̼ԭ�Ӻ���ԭ�ӵĸ�����Ϊ1��2
�ο��𰸣�B
�����������������֪���û����ᄃ������C-O���Ϊһ�ֿռ���״����������ṹ�����Ըû���������ԭ�Ӿ��壬�;����������Ľṹ���ƣ����þ�̯��ȷ���仯ѧʽ������ԭ�Ӿ�������ʷ�����ɡ�A���û����ᄃ����ÿ��̼ԭ�Ӿ����ĸ����۵�������ԭ�ӽ��Ϊһ�ֿռ���״��������չ�ṹ�������ڷ��ӣ�����ԭ�Ӿ��壬��A��ȷ��B���þ����У�ÿ��̼ԭ�Ӻ���4��C-O���ۼ�������Cԭ����C-0��ѧ����Ŀ֮��Ϊ1��4����B����C���þ���Ŀռ���С����6��̼ԭ�Ӻ�6����ԭ�ӹ��ɣ���˾���Ŀռ���С������12��ԭ�ӹ��ɣ���C��ȷ��D��������ÿ��̼ԭ�Ӿ����ĸ����۵�������ԭ�ӽ�ϣ�ÿ����ԭ�Ӻ�2��̼ԭ���Թ��۵������ϣ�����̼��ԭ�Ӹ����ȣ�1:2����D��ȷ����ѡB��
�����Ѷȣ�һ��
2��ѡ���� ���ۼ������Ӽ��ͷ��»�����������֮��IJ�ͬ����������������ͬʱ������������������������ǣ�������?
��Na2O2����SiO2����ʯī���ܽ��ʯ����NaCl���ް���?
A���٢ڢ�
B���٢ۢ�
C���ڢܢ�
D���ۢܢ�?
�ο��𰸣�B?
���������Na2O2��Na+��O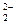 ֮�������Ӽ���ϣ�O
֮�������Ӽ���ϣ�O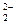 ��O��O�Թ��ۼ���ϣ�����������ʯī��ÿһ������̼̼����ϣ������֮���Է��Ӽ���������ϣ���������������(P4��������P��P�Թ��ۼ���ϣ���P4����֮���Է��Ӽ�����ϣ�Ҳ�������⣻SiO2�����ʯֻ�й��ۼ���Ϊԭ�Ӿ��壬NaCl��ֻ�����Ӽ���?
��O��O�Թ��ۼ���ϣ�����������ʯī��ÿһ������̼̼����ϣ������֮���Է��Ӽ���������ϣ���������������(P4��������P��P�Թ��ۼ���ϣ���P4����֮���Է��Ӽ�����ϣ�Ҳ�������⣻SiO2�����ʯֻ�й��ۼ���Ϊԭ�Ӿ��壬NaCl��ֻ�����Ӽ���?
�����Ѷȣ�һ��
3��ѡ���� ���нṹͼ�У������ǰ������Ԫ�ص�ԭ��ʵ��ԭ��ʵ��ԭ�ӳ�ȥ�������Ӻ�ʣ��IJ��֣���С�ڵ����δ�����γɹ��ۼ����������ӣ����ߴ������ۼ���ʾ����F2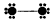 ���ݸ�ͼ��ʾ�Ľṹ�ص㣬�����й�������ȷ����
���ݸ�ͼ��ʾ�Ľṹ�ص㣬�����й�������ȷ����

[? ]
A�������ṹͼ�й�����6��Ԫ��
B���ס��ҡ���Ϊ�Ǽ��Է��ӣ���Ϊ���Է���
C�����붡���Է������Ϸ�Ӧ�������ӻ�����
D����CaCl2��Һ�м��루��ͨ�룩���а�ɫ��������
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4������� (10��)��A��B��C��D��E��F����Ԫ�أ���֪������λ��������ͬ�����ڣ��˵������������A��E��B��F�ֱ�ͬ���壻A��E�ֱ�����D��ԭ�Ӹ�����1�s1��2�sl�γɻ����B��C�ֱ�����D��ԭ�Ӹ�����1�s1��1�s2�γɻ����
��д��ֻ����A��B��D��E����Ԫ�ص����ֳ�����ˮ�εĻ�ѧʽ_____________��
����ͼ��A��D�γɵ�һ�ֻ�����ľ���ṹʾ��ͼ�����е����߱�ʾ__________��E��D��ԭ�Ӹ�����1�s1�γɵĻ�����ĵ���ʽΪ_____________________��
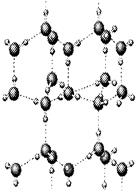
������ͨ���Ѳ�l molij��ѧ�������յ��������ɸ�
��ѧ���ļ��ܡ����ܵĴ�С���Ժ�����ѧ����ǿ����Ҳ����
 ���ڹ��㻯ѧ��Ӧ�ķ�Ӧ��(��H)����ѧ��Ӧ�ġ�H���ڷ�Ӧ
���ڹ��㻯ѧ��Ӧ�ķ�Ӧ��(��H)����ѧ��Ӧ�ġ�H���ڷ�Ӧ
�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮��
�IJ�±��г�����������Ԫ���γɵĻ�ѧ���ļ��ܣ�
��ѧ��
| F��D
| F��F
| B��B
| F��B
| C�TD
| D�TD
|
����/kJ��mol��1
| 460
| 176
| 347.7
| 347
| 745
| 497.3
|
���������������γɵľ��壬�۵��ɸߵ��͵�˳��(��a��b��c��ʾ)��_________��
a��F��B�γɵĻ�����? b��B��D�γɵ��ȶ�������? c��F�ĵ���
���Թ���F���ʾ����ȼ���ȣ�____________________________________��
�ο��𰸣�(1)NaHCO3��CH3COONa? (2)���?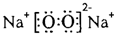
(3) �� a>c>b?��990.7 kJ/mol
�������������Ԫ�����ڱ��Ľṹ��������жϼ��йط�Ӧ�ȵļ��㡣
��������Ԫ�ص����ʿ��жϣ�A��H��B��C��C��N��D��O��E��Na��F��Si��
��1��ֻ����H��C��O��Na����Ԫ�ص����ֳ�����ˮ�ηֱ�Ϊ̼���ƺʹ����ơ�
��2��H��O�γɵij�����������ˮ��ˮ�д���������������߱�ʾ�����Na��O��ԭ�Ӹ�����1�s1�γɵĻ������ǹ������ƣ��������Ӽ��ͷǼ��Լ���
��3����a��SiC����ԭ�Ӿ��壬b��CO2���Ƿ��Ӿ��壬c��Si��Ҳ��ԭ�Ӿ��塣��ΪSi��C�ļ��ܴ���Si��Si�ļ��ܣ�����̼������۵���ڹ�ģ���ĸ���CO2�ģ���a>c>b��
�ڹ��������Ӧ�Ļ�ѧ����ʽΪSi��O2=SiO2����Ϊ1����ԭ���γ�2��Si��Si���ڶ������辧����1����ԭ���γ�4��Si��O�����Ը÷�Ӧ��ȼ������2��176 kJ��mol��1+497.3 kJ��mol��1��4��460 kJ��mol��1��990.7 kJ/mol��
�����Ѷȣ�һ��
5������� ����������һ�ֽྻ����������Դ��������������Ҫ�ɷ�ΪCO��CO2��H2�ȣ���H2��ϣ����ϳɼ״��������������õķ���֮һ��
(1)������Ӧ�Ĵ�������Cu��Zn��Al��Ԫ�ء�д����̬Znԭ�ӵĺ�������Ų�ʽ__________��
(2)���ݵȵ���ԭ����д��CO���ӵĽṹʽ________��
(3)�״��������ɵõ���ȩ����ȩ������Cu(OH)2�ļ�����Һ��Ӧ����Cu2O������
�ټ״��ķе�ȼ�ȩ�ĸߣ�����Ҫԭ����________ ����ȩ������̼ԭ�ӹ�����ӻ�����Ϊ________��
�ڼ�ȩ���ӵĿռ乹����________��1 mol��ȩ�����ЦҼ�����ĿΪ_______��
����1��Cu2O�����У��ṹ����ͼ��ʾ������������Cuԭ����ĿΪ______��
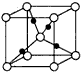
�ο��𰸣�(1)1s22s22p63s23p63d104s2��[Ar]3d104s2
(2)C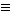 O
O
(3)�ټ״�����֮���γ������sp2�ӻ�����ƽ�������Σ�3NA����4
���������
�����Ѷȣ�һ��