微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 (10分)钾是活泼的碱金属,钾和氧有氧化钾(K2O)、过氧化钾(K2O2)和超氧化钾(KO2)等多种化合物。
⑴钾和硝酸钾反应可制得氧化钾:K+KNO3→K2O+N2(未配平),每生成9.4gK2O消耗的还原剂有___________g
⑵超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂。写出超氧化钾与二氧化碳反应的化学方程式_____________________________,为了维持气压稳定,可以使用超氧化钾和过氧化钾的混合物使吸收的CO2与生成的O2体积相同(同温同压),则它们的物质的量之比为n(KO2) : n(K2O2)=____________
⑶KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比。如果产物A只含有两种化合物,写出所有可能的化学式并计算A中两种化合物的物质的量之比。
参考答案:(10分)1)6.5g(2分)(2)4KO2+2CO2→2K2CO3+3O2;(2分)? 2:1(2分)
(3)2:3 (2分)? K2O2和KO2?1:2?(1分)? K2O与KO2?1:4(1分)
本题解析:略
本题难度:一般
2、选择题 下列关于碳酸氢钠的叙述,不正确的是(?)
A.它是一种白色粉末,易溶于水
B.其分子式为NaHCO3・10H2O,在空气里易风化
C.可以跟氢氧化钠起反应,生成正盐
D.与碳酸钠相比,若质量相同,分别跟足量的盐酸反应,碳酸氢钠得到的CO2多
参考答案:B
本题解析:碳酸氢钠是一种酸式盐。在钠盐中,不管是酸式盐还是正盐均易溶于水,故NaHCO3与食盐相似,是白色粉末,可溶于水,A项正确。NaHCO3的分子中不含结晶水,在空气里也没有易风化的性质,B项不正确。NaHCO3可以和NaOH反应,NaHCO3+NaOH====Na2CO3 +H2O,C项正确。D项正确,因此设各取106 g,则
Na2CO3+2HCl====2NaCl+H2O+CO2↑
106? 44
106 g? x
x="44" g
NaHCO3+HCl====NaCl+H2O+CO2↑
84? 44
106 g? y
y="55.5" g
本题难度:一般
3、填空题 有人设计了如右图的实验装置,目的是做钠与水反应的实验并验证:①钠的物理性质;②钠与水反应的产物。
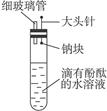
(1)为了完成他的实验,还需要的仪器有___________________________________________。
(2)假如已按如图所示装配好了仪器,接下来的操作是______________________________。
(3)实验现象是________________________________________________________________。
参考答案:(1)小试管、酒精灯(2)将大头针向上提,使钠块从针头脱落并落入水中,将小试管扣在导管上收集反应产生的气体,用拇指堵住试管口移近酒精灯,松开拇指点燃试管中的气体
(3)钠浮在水面上,很快熔化成闪亮的小球,并逐渐消失,水溶液由无色变成红色;反应有气体生成,点燃小试管中的气体时,有尖锐的爆鸣声
本题解析:(1)钠与水反应的化学方程式为:2Na+2H2O====2NaOH+H2↑。生成的NaOH能通过滴有酚酞的水溶液变红来检验,生成的H2则应该收集后再进行点燃实验,故还需要用到小试管和酒精灯。(2)接下来的操作是让钠与水接触开始反应,并观察现象、收集和验证产生的气体是否是氢气。
本题难度:简单
4、选择题 下列试剂的保存或使用正确的是(?)
A.金属锂保存在煤油中,取出使用前要用滤纸吸干煤油
B.过氧化钠比氧化钠稳定,可露置在空气中
C.称量NaOH固体时,可在天平两个托盘上各放一张等质量的纸,左边纸上放NaOH,右边纸上放砝码
D.做焰色反应实验时,透过蓝色钴玻璃,观察到火焰颜色为紫色,证明被检验物中一定有钾元素
参考答案:D
本题解析:金属锂由于密度小,不能保存在煤油中;Na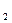 O
O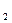 由于与空气中的H
由于与空气中的H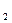 O或CO
O或CO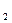 能反应,所以不能露置在空气中;NaOH有腐蚀性,易潮解,不能放在纸上称量;蓝色钴玻璃可以滤去黄色的光。
能反应,所以不能露置在空气中;NaOH有腐蚀性,易潮解,不能放在纸上称量;蓝色钴玻璃可以滤去黄色的光。
本题难度:简单
5、填空题 联碱法(侯氏制碱法)和氨碱法的生产流程简要表示如下图:
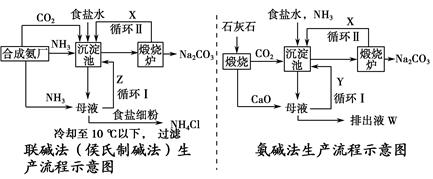
(1)沉淀池中发生反应的化学方程式为________________。
(2)X是________,Y是________(填化学式)。
(3)Z中除了溶解的氨气、食盐外,其它溶质还有________________;排出液W中的溶质除了氢氧化钙外,还有________________。
(4)从理论上分析,在氨碱法生产过程中________(填“需要”或“不需要”)补充氨气。
(5)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确是________(填序号)。
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气目的是使氯化铵更多析出
c.加入食盐细粉目的是提高Na+的浓度,促进碳酸氢钠结晶析出
(6)联碱法与氨碱法相比,指出联碱法的一项优点___________________。
参考答案:(1)NaCl+NH3+H2O+CO2=NaHCO3↓+NH4Cl (2)CO2 NH3
(3)NaHCO3、NH4Cl CaCl2、NaCl (4)不需要 (5)b (6)不产生无用的CaCl2(或提高了食盐的转化率等)。
本题解析:(1)两种方法中沉淀池内产生的物质均为NaHCO3和NH4Cl且析出的均
是NaHCO3,发生的反应是NH3+H2O+NaCl+CO2=NaHCO3↓+NH4Cl。
(2)两种方法中煅烧炉内发生的反应均是:2NaHCO3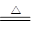 ?Na2CO3+CO2↑+H2O↑,可见循环的X是CO2。氨碱法中:向母液加入CaO后,生成NH3循环利用,排出液W中含有CaCl2及未反应的NaCl、Ca(OH)2等。
?Na2CO3+CO2↑+H2O↑,可见循环的X是CO2。氨碱法中:向母液加入CaO后,生成NH3循环利用,排出液W中含有CaCl2及未反应的NaCl、Ca(OH)2等。
(3)联碱法中,母液中含有NaCl、NH3、NH4Cl(少量)、NaHCO3(少量)。
(4)从理论上分析,氨碱法生产中的母液主要含有NH4Cl、NaHCO3,加入过量CaO后,NH4Cl与Ca(OH)2反应生成NH3,显然不用补充氨气。
(5)增大母液中c(NH4+)和c(Cl-)均可以使NH4Cl析出。
本题难度:一般