微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关钠的叙述正确的是
A.钠在空气中燃烧生成氧化钠
B.钠元素在自然界中可以以游离态形式存在
C.少量金属钠可以保存在煤油中
D.金属钠投入硫酸铜溶液中有铜生成
参考答案:C
本题解析:A、钠在空气中燃烧生成过氧化钠,错误;B、钠化学性质活泼,易与空气中的水、氧气反应,在自然界中只能以化合态存在,错误;C、少量金属钠可以保存在煤油中,正确;D、金属钠投入硫酸铜溶液中,钠先与水反应生成氢氧化钠和氢气,氢氧化铜再与硫酸铜溶液中反应生成氢氧化铜,错误。
本题难度:一般
2、选择题 在一定温度下,向饱和的烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到室温,下列说法正确的是
[? ]
A.溶液中Na+浓度增大,有O2放出
B.溶液中OH-浓度不变,有H2放出
C.溶液中Na+数目减少,有O2放出
D.溶液中OH-浓度增大,有O2放出
参考答案:C
本题解析:
本题难度:一般
3、填空题 (6分)(1)Na2O2可用在潜水艇里作为氧气的一种来源,供人们呼吸所需。Na2O2所发生反应的化学方程式为?
(2)钠和水反应的化学方程式?
(3)铝和氢氧化钠溶液反应的化学方程式?
参考答案:(1) 2Na2O2+2CO2=2Na2CO3+O2
(2)2Na+2H2O=2NaOH+H2↑
(3) 2 Al+2NaOH+2H2O=" 2" NaAlO2+3H2↑
本题解析:(1)过氧化钠能和CO2反应生成碳酸钠和氧气,所以可以作为供氧剂,反应的方程式是2Na2O2+2CO2=2Na2CO3+O2。
(2)钠极易和水反应生成氢氧化钠和氢气,反应的方程式是2Na+2H2O=2NaOH+H2↑。
(3)金属铝能和强碱溶液反应生成氢气,反应的化学方程式是2 Al+2NaOH+2H2O=" 2" NaAlO2+3H2↑。
点评:该题属于基础性试题,关键是记住常见物质的化学性质及其相应的方程式。
本题难度:一般
4、选择题 0.5 mol Na、Mg、Al分别与100 mL 0.5 mol・L-1的盐酸充分反应,下列关于所得气体在同温同压下的体积关系中,正确的是(?)
A.相同
B.铝最多,钠最少
C.铝最多,镁和钠相同
D.钠最多,镁和铝相同
参考答案:D
本题解析:Na、Mg、Al都能与盐酸反应,从给出的量可知三种金属均是过量的,但过量的钠还能与水反应,因此钠产生的H2最多,而Mg和Al产生的H2一样多。
本题难度:简单
5、填空题 我国濒临海域的省份,能够充分利用海水制得多种化工产品。下图是以海水、贝壳(主要成分CaCO3)等为原料制取几种化工产品的工艺流程图,其中E是一种化肥,N是一种常见的金属单质。
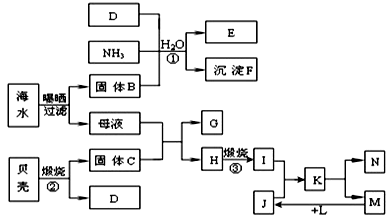
结合上述工艺流程回答下列问题:
(1)物质G和L的化学式分别为?和???;固体B是生活中的一种必需品,主要用作 ??
(2)上述工艺流程中可以循环使用的物质的化学式为??
(3)反应①的化学方程式为?;在反应①中必须先通入NH3,而后通入D,其原因是?
(4)工业上利用F可制得另一种化工产品,该反应的化学方程式为?
(5)由K溶液经如何处理才能制得N??
参考答案:(1)CaCl2? H2?调味品
(2)CO2
(3)NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl? NH3在溶液中的溶解度大,利于吸收CO2,使其转化为(NH4)2CO3
(4)2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(5)MgCl2溶液必须在氯化氢气体中进行蒸发结晶制得MgCl2晶体,熔融电解可制取金属镁
本题解析:贝克高温煅烧得到CaO和CO2。海水曝晒得到NaCl固体和含有CaCl2、MgCl2的母液。NaCl、CO2、NH3在水溶液中发生反应:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl产生小苏打沉淀。滤液中含有NH4Cl。将CaO加入含有MgCl2溶液中,发生反应:CaO+ MgCl2+H2O=Mg(OH)2↓+ CaCl2. 将过滤出来,洗涤干净,然后灼烧Mg(OH)2,发生分解反应Mg(OH)2 MgO+ H2O。用HCl溶解MgO,得到纯净的MgCl2溶液。将该溶液蒸发、浓缩,冷却结晶得到MgCl2・6H2O.将MgCl2・6H2O加热,在HCl的气氛中加热蒸发得到无水MgCl2。然后电解熔融的Mg Cl2即得到Mg和Cl2.(1)物质G和L的分别为CaCl2和H2。固体NaCl是生活中的一种必需品,主要用作调味品。(2)上述工艺流程中可以循环使用的物质的化学式为CO2。(3)反应①的化学方程式为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。在反应①中必须先通入NH3,而后通入CO2,是因为NH3在溶液中的溶解度大,利于吸收CO2,使其转化为(NH4)2CO3。(4)工业上利用NaHCO3可制得另一种化工产品Na2CO3,该反应的化学方程式为2NaHCO3
MgO+ H2O。用HCl溶解MgO,得到纯净的MgCl2溶液。将该溶液蒸发、浓缩,冷却结晶得到MgCl2・6H2O.将MgCl2・6H2O加热,在HCl的气氛中加热蒸发得到无水MgCl2。然后电解熔融的Mg Cl2即得到Mg和Cl2.(1)物质G和L的分别为CaCl2和H2。固体NaCl是生活中的一种必需品,主要用作调味品。(2)上述工艺流程中可以循环使用的物质的化学式为CO2。(3)反应①的化学方程式为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。在反应①中必须先通入NH3,而后通入CO2,是因为NH3在溶液中的溶解度大,利于吸收CO2,使其转化为(NH4)2CO3。(4)工业上利用NaHCO3可制得另一种化工产品Na2CO3,该反应的化学方程式为2NaHCO3 Na2CO3+ CO2↑+H2O。(5)MgCl2是强酸弱碱盐,加热发生水解反应得到Mg(OH) 2和HCl,HCl容易挥发,导致得到的固体为Mg(OH) 2。为了抑制其水解,所以必须在氯化氢气体中进行蒸发结晶制得无水MgCl2,然后电解熔融氯化镁,可制取金属镁。
Na2CO3+ CO2↑+H2O。(5)MgCl2是强酸弱碱盐,加热发生水解反应得到Mg(OH) 2和HCl,HCl容易挥发,导致得到的固体为Mg(OH) 2。为了抑制其水解,所以必须在氯化氢气体中进行蒸发结晶制得无水MgCl2,然后电解熔融氯化镁,可制取金属镁。
本题难度:一般