微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 X、Y、Z都是金属,把X放入Z的盐溶液中,X的表面附着一层Z;X与Y组成原电池时,X为电池的正极。X、Y、Z三种金属的活动性顺序是
A.X>Y>Z
B.X>Z>Y
C.Y>X>Z
D.Y>Z>X
参考答案:C
本题解析:略
本题难度:简单
2、选择题 根据下图,下列判断中正确的是
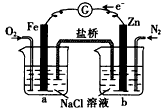
[? ]
A.烧杯a中的溶液pH 升高
B.烧杯b中发生氧化反应
C.烧杯a中发生的反应为2H++2e-=H2
D.烧杯b中发生的反应为2Cl--2e-=Cl2
参考答案:AB
本题解析:
本题难度:一般
3、选择题 已知: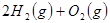
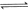

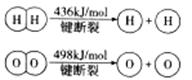
下列说法不正确的是
A.该反应原理可用于设计氢氧燃料电池
B.破坏1molH-O键需要的能量是463.4kJ
C.H2O(g)=H2(g)+1/2O2(g)△H="+241.8" kJ/mol
D.H2(g)中的H-H键比H2O(g) 中的H-O键牢固
参考答案:D
本题解析:原电池中必须有电子的转移,所以只有氧化还原反应才能设计成原电池,A正确。反应热是断键吸收的能量和形成化学键所放出的能量的差值,因此有2×436kJ/mol+498kJ/mol-2×2×akJ/mol=-483.6kJ/mol,解得a=463.4,所以选项B正确。正反应是放热反应,则逆反应就是吸热反应,C正确。化学键越强越牢固,因此根据键能可知,水中H-O比氢气中H-H键牢固,D不正确,答案选D。
本题难度:一般
4、填空题 (9分)下图是一个甲 烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
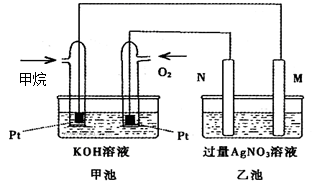
(1)M电极的材料是?,N的电极电极反应式为:?;乙池的总反应式是?,通入甲烷的铂电极上发生的电极反应式为?__________________________?。
(2)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为??L(标准状况下);若此时乙池溶液的体积为400mL,则乙池中溶液的H+的浓度为???。
参考答案:(9分)(1)?铁?,? 4 OH- - 4 e-? = O2 ↑ + 2H2O ,
4AgNO3+2H2O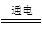 ?4Ag+ O2↑+4HNO3, CH4-8e-+10OH-= CO32-+7H2O 。
?4Ag+ O2↑+4HNO3, CH4-8e-+10OH-= CO32-+7H2O 。
(2)? 0.224 L,? 0.1mol/L?(每空1分)
本题解析:(1)甲是燃料电池,通入甲烷的电极是负极,通入氧气的是正极。所以M是阴极,N是阳极。由于工作时M、N两个电极的质量都不减少,所以M是铁,N是石墨,溶液中OH-放电,所以其电极反应式是4 OH- - 4 e- = O2 ↑ + 2H2O,则乙池中总的反应式是4AgNO3+2H2O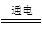 ?4Ag+ O2↑+4HNO3。由于原电池中电解质溶液显碱性,所以负极的电极反应式是CH4-8e-+10OH-= CO32-+7H2O 。
?4Ag+ O2↑+4HNO3。由于原电池中电解质溶液显碱性,所以负极的电极反应式是CH4-8e-+10OH-= CO32-+7H2O 。
(2)4.32g银的物质的量是0.04mol,则转移电子是0.04mol。所以根据电子的得失守恒可知,消耗0.01mol氧气,标准状况下的途径是0.224L。根据乙池中的总反应式可知,此时生成硝酸是0.04mol,所以氢离子的浓度是0.04mol÷0.4L=0.1mol/L。
本题难度:一般
5、选择题 镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低、燃料易于贮运等特点。研究的燃料电池可分为镁―空气燃料电池,镁―海水燃料电池,镁―过氧化氢燃料电池,镁―次氯酸盐燃料电池。如图为镁―次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是( )。
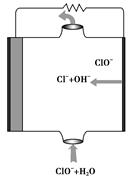
A.放电过程中OH-移向正极
B.电池的总反应式为Mg+ClO-+H2O=Mg(OH)2↓+Cl-
C.镁电池中镁均为负极,发生氧化反应
D.镁―过氧化氢燃料电池,酸性电解质中正极反应为:H2O2+2H++2e-=2H2O
参考答案:A
本题解析:根据图像判断反应过程,判断正、负极,正确书写电极反应式。镁燃料电池,镁作负极失电子,产物由电解质溶液决定,若为酸性溶液生成Mg2+,碱性溶液生成Mg(OH)2。ClO-在正极反应,由图可知有Cl-和OH-生成,OH-向负极移动,生成Mg(OH)2。
本题难度:一般