��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��8NH3+3Cl2====6NH4Cl+N2��Ӧ�У�����2 mol N2���ɣ�����������Ӧ��NH3�����ʵ����� (? )
A��16 mol
B��8 mol
C��4 mol
D��3 mol
�ο��𰸣�C
������������ݷ�Ӧʽ���жϣ�3mol����ȫ��������������Ҫ�õ�6mol���ӡ����ݵ�ʧ�����غ��֪�����Ա������İ�����2mol�����ɵ�����1mol���������2 mol N2���ɣ�����������Ӧ��NH3�����ʵ�����4mol���������õ�ԭ���غ㣬��Ϊ����������������ݵ�ԭ���غ��֪���±������İ�����Խ����4mol����ѡC��
�����Ѷȣ�һ��
2������� ������ʳ�ι�ϵ���У�ʳ�����ϰ���������ִ����Ĺ�ũҵ�����о�����Ҫ���ã������к���Ca2+��Mg2+��SO42-�Լ���ɳ�����ʣ���ش�����ᴿ���й����⣺
��1��Ϊ�˳�ȥ�����е���ɳ���ɲ�ȡ���ᴿʵ�����������������______��
��2��Ϊ�˳�ȥ���������ʣ���������ʵ�鲽������ᴿ���ټӹ���BaCl2��Һ���ڼӹ���NaOH��Һ���ۼӹ���Na2CO3��Һ���ܹ��ˣ���______���벹ȫʵ�鲽�裬���ش���۵�Ŀ����______��
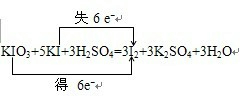
��3��2010��7��26�գ������������ˡ�ʳ���ε⺬��������������壬��������������������ʳ�����е⺬��ƽ��ˮƽ�Ĺ涨�������ͣ�ʳ�������ӵ���KIO3���������з�Ӧ������ʳ�����Ƿ�KIO3��KIO3+KI+H2SO4-I2+K2SO4+H2O?��δ��ƽ��������ƽ�÷�Ӧ����ʾ������ת�Ƶķ������Ŀ______��Ϊ�˻�ȡ��Ӧ����Һ�е�I2���ɲ�ȡ��ʵ�����������������______��
�ο��𰸣���1�������Ƚ����κ����е���ɳ�ܽ���ˮ���Ȼ�����������ˮ�ģ�����ɳ��������ˮ�ģ��������Һ��ķ�����Բ��ù��˷������ʴ�Ϊ���ܽ⡢���ˣ�
��2���ڴ����ᴿʱ��Ҫ�����һ���������ᣬ��ȥ���������������Ӻ�̼������ӣ�����̼���Ƶ�Ŀ���dz�ȥ�����ӺͶ���ı����ӣ��ʴ�Ϊ�����������?��ȥCa2+������Ba2+��
��3�����ݵ����غ��ԭ���غ�����ƽ����ʽ����������ԭ��ӦKIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O�У����ϼ�����ֵ=���ϼ۽���ֵ=ת�Ƶ�����=6������ת��������£�
���ⵥ�ʴӵ�ˮ����ȡ���Բ�����ȡ��Һ�����������Ȼ�̼����ȡ��Ȼ��������Ȼ�̼�͵�ķе�IJ�ͬ�����룬
�ʴ�Ϊ��

����ȡ������
���������
�����Ѷȣ�һ��
3������� ��ƽ���з���ʽ��
(1)C+H2SO4��Ũ��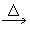 CO2��+SO2��+H2O______________________
CO2��+SO2��+H2O______________________
(2)Cu+ HNO3(ϡ)��Cu(NO3)2+NO��+H2O______________________
(3)NH3+O2 NO+H2O______________________
NO+H2O______________________
�ο��𰸣�(1)C+2H2SO4(Ũ) CO2��+2SO2��+2H2O
CO2��+2SO2��+2H2O
(2)3Cu+8HNO3(ϡ)=3Cu(NO3)2+2NO��+4H2O
(3)4NH3+5O2 4NO+6H2O
4NO+6H2O
���������
�����Ѷȣ�һ��
4������� �л���ѧ�г���18Oԭ����ʾ��ԭ�����о��������Ҵ���Ӧ�������ķ�Ӧ��������Ӧ����������Ӷ���C��O�����������Ӷ���O��H����������дCH3COOH��CH3CH218OH��Ӧ�Ļ�ѧ����ʽ��?
��֪��Ӧ: KClO3 + 6HCl =" KCl" + 3Cl2 + 3H2O ,����K35ClO3��H37Cl����,��������������Է�������Ϊ? .
�ο��𰸣�CH3COOH��CH3CH218OH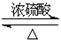 CH3CO18OCH2CH3��H2O��73.33
CH3CO18OCH2CH3��H2O��73.33
�����������������Ӧ�������ṩ�ǻ������ṩ��ԭ�ӣ����Ը÷�Ӧ�ķ���ʽӦ����CH3COOH��CH3CH218OH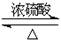 CH3CO18OCH2CH3��H2O���ڷ�ӦKClO3 + 6HCl =" KCl" + 3Cl2 + 3H2O��������������ء���ԭ�����Ȼ��ء������������ͻ�ԭ�������ʵ���֮����1�U5�����������K35ClO3��H37Cl���ã�������������35Cl��37Clԭ�Ӹ���֮����1�U5��������Ԫ�ص�ƽ�����ԭ��������1/6��35+5/6��37��36.67������������ӵ����ʵ�����36.67��2��73.33��
CH3CO18OCH2CH3��H2O���ڷ�ӦKClO3 + 6HCl =" KCl" + 3Cl2 + 3H2O��������������ء���ԭ�����Ȼ��ء������������ͻ�ԭ�������ʵ���֮����1�U5�����������K35ClO3��H37Cl���ã�������������35Cl��37Clԭ�Ӹ���֮����1�U5��������Ԫ�ص�ƽ�����ԭ��������1/6��35+5/6��37��36.67������������ӵ����ʵ�����36.67��2��73.33��
��������������ԭ��Ӧ�У������ͬһ��Ԫ�صĸ�̬��ͼ�̬֮�䷢��������ԭ��Ӧ�������ļ�ֻ̬�ܴ����м䣬����������ļ�̬�����ڻ�ԭ����ģ��ݴ˿����жϻ�ԭ������������
�����Ѷȣ�һ��
5��ѡ���� (NH4)2SO4�ڸ����·ֽ⣬������SO2��H2O��N2��NH3���ڸ÷�Ӧ�Ļ�ѧ����ʽ�У���ѧ��������С����IJ������������
A��SO2��H2O��N2��NH3
B��H2O��SO2��N2��NH3
C��N2��SO2��NH3��H2O
D��H2O ��NH3��SO2��N2
�ο��𰸣�C
���������(NH4)2SO4�ڸ����·ֽ⣬������SO2��H2O��N2
����(NH4)2SO4--------> N2 + SO2 + NH3 + H2O
NH4+��-3 ��0,ʧȥ3�����ӣ�����N2���Ӻ�����N������ʧȥ3��2=6�����ӡ�
SO42-��+6��+4�õ�2�����ӣ�����SO42-��3���õ�3��2=6�����ӡ�
3(NH4)2SO4��N2 + 3SO2 + NH3 + H2O
������һ���Ͳ�ࡣ��6��NH4+����2��ת��ΪN2��ʣ��4��û�з���������ԭ��Ӧ�����ǣ�
3(NH4)2SO4�� N2 + 3SO2 +4NH3 + H2O��Ȼ�����һ�����������3��(4��2)-4��3=12��
����H2O��6������ȻҲ������SO42-ʧȥ�������㡣
���յõ���
3(NH4)2SO4==����="=" N2 + 3SO2 +4NH3 + 6H2O����ѡC��
���������⿼�����������ԭ��Ӧ��Ӧ�ã�����Ҫ���ݵ���ת���غ㼴���ϼ����߽���һ������ƽ��
�����Ѷȣ�һ��