��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������һ����Դ��������Ҫ�ɷ���CH4��0��5molCH4��ȫȼ������CO2��H2Oʱ���ų�445kJ�������������Ȼ�ѧ����ʽ����ȷ����
[? ]
A��2CH4��g����4O2��g����2CO2��g����4H2O��l�� ��H����890kJ��mol-1
B��CH4��g����2O2��g����CO2��g����2H2O��l�� ��H����890kJ��mol-1
C��CH4��g����2O2��g����CO2��g����2H2O��l�� ��H����890kJ��mol-1
D��1/2CH4��g����O2��g����1/2CO2��g����H2O��l�� ��H����890kJ��mol-1
�ο��𰸣�C
���������
�����Ѷȣ���
2������� �������Ļ������ڹ�ҵ�������ճ������ж��й㷺����;��
��1���ڶ������У�������������������Ӧ�ų����������и�ֽ�÷�Ӧ�Ļ�ѧ����ʽΪ______��
��2����֪2FeO3��s��+3C��s���T3CO2��g��+4Fe��s����H=+468.2kJ?mol-1��C��s��+O2��g���TCO2��g����H=-393.5kJ?mol-1����Fe��s����O2��g����Ӧ����Fe2O3��s�����Ȼ�ѧ����ʽΪ______��
��3������KMnO4��Һ�ζ�Fe2+��Ũ�ȣ���Ӧ�����ӷ���ʽ���£�5Fe2++MnO4-+8H+�T5Fe3++Mn2++4H2O
��KMnO4��ҺӦʢ����______�ζ����У�
���жϴﵽ�ζ��յ��������______��
���������ữ��0.02000mol?L-1 KMnO4��Һ�ζ�ijFeSO4��Һ���յ㣬ʵ�����ݼ�¼���±���
| �ζ���� | ����Һ����MmL | ����KMn0��Һ����MmL
1
25.00
19.98
2
25.00
19.12
3
25.00
20.02
|
��������ݲ����㣬��FeSO4��Һ�����ʵ���Ũ��Ϊ______��
��4���������ײ���ZnFe2Ox�������ڳ�ȥ��ҵ�����е�ijЩ�������ȡ�²��Ϻͳ�ȥ������ת����ϵ��ͼ��

����֪ZnFe2O4��H2��Ӧ�����ʵ���֮��Ϊ2��1����ZnFe2Ox��x=______��
����ZnFe2Ox��ȥSO2�Ĺ����У���������______��
�ο��𰸣���1�������������ڵ�ȼ�����������������������������Ҹ÷�Ӧ�ų��˴������ȣ���Ӧ����ʽΪ2Al+Fe2O3����.2Fe+Al2O3��
�ʴ�Ϊ��2Al+Fe2O3����.2Fe+Al2O3��
��2����2Fe2O3��s��+3C��s���T3CO2��g��+4Fe��s����H=+468.2kJ?mol-1��
��C��s��+O2��g���TCO2��g����H=-393.5kJ?mol-1
���ݸ�˹���ɣ��ڡ�3-�ٵã�4Fe��s��+3O2��g���T2Fe2O3��s��
��H=3����-393.5kJ?mol-1��-468.2kJ?mol-1=-1648.7kJ?mol-1��
�ʴ�Ϊ��4Fe��s��+3O2��g���T2Fe2O3��s����H=-1648.7kJ?mol-1��
��3����KMnO4��Һ����ǿ�����ԣ����Ը�ʴ��Ƥ�ܣ�Ӧװ����ʽ�ζ����У��ʴ�Ϊ����ʽ��
��FeSO4��Ӧ��ϣ��������һ��KMnO4��Һ����Һ��Ϊdz�Ϻ�ɫ��dz�Ϻ�ɫ������ڲ���ȥ��˵���ζ����յ㣬
�ʴ�Ϊ����Һ��Ϊdz�Ϻ�ɫ���Ұ�����ں�ɫ����ȥ��
��2��KMnO4��Һ��������1��3�����Ƚϴ�Ӧ�����Ӧ����1��3���������KMnO4��Һ�������
������KMnO4��Һ�����Ϊ19.98+20.022mL=20mL����FeSO4��Һ��Ũ��Ϊcmol/L��
��KMnO4��5FeSO4��֪��5��20mL��0.02000mol?L-1=25mL��cmol/L�����c=0.0800��
�ʴ�Ϊ��0.0800mol?L-1��
��4����ZnFe2O4��H2��Ӧ�����ʵ���֮��Ϊ2��1����ZnFe2OX����Ԫ�صĻ��ϼ�Ϊa�����ݵ���ת���غ㣬
��֪2mol��2����3-a��=1mol��2����ã�a=2.5�����û��ϼ۴�����Ϊ�㣬2+2.5��2=2x�����x=3.5���ʴ�Ϊ��3.5��
���������ײ���ZnFe2OX���ɻ�����ZnFe2O4�����»�ԭ�Ƶã���ZnFe2OX��SO2��Ӧ�õ�ZnFe2O4���������Ļ��ϼ����ߣ�Ҳ���ɢټ����֪����ZnFe2OX����ԭ������SO2�����������ʴ�Ϊ��SO2��
���������
�����Ѷȣ�һ��
3������� ��20�֣����������������ܵ�����Խ��Խ��Ĺ�ע����Ҫ��ش��������⣺
��ʵ�ַ�ӦCH4(g)+CO2(g) 2CO(g)+2H2(g)����H0���Լ������������ŷźͼ���ȼ��Σ��������Ҫ���塣��2L�ܱ������У�ͨ��5mol CH4��5mol CO2�Ļ�����壬һ�������·���������Ӧ�����CH4��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��
2CO(g)+2H2(g)����H0���Լ������������ŷźͼ���ȼ��Σ��������Ҫ���塣��2L�ܱ������У�ͨ��5mol CH4��5mol CO2�Ļ�����壬һ�������·���������Ӧ�����CH4��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��

��p1��p2��p3��p4�ɴ�С��˳�� ���÷�Ӧ������Ӧ��______(����ȡ����ȡ�)��Ӧ����1000������ת����Ϊ80%ʱ���÷�Ӧ��ƽ�ⳣ��K=________��
��PM2.5��Ⱦ��ֱ���ŷŻ�ʯȼ�ղ����������йأ���ʯȼ��ȼ��ͬʱ�ų�������SO2��NOx��
��1������NOx��һ�ַ��������ü������ԭNOx��
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ��H1=��574kJ��mol��1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ��H2=��1160kJ��mol��1
CH4(g)+2NO2 (g)= N2(g) + CO2(g)+2H2O(g) ��H3
���H3= �����������Ӧ��ƽ�ⳣ������ΪK1��K2��K3����K3=__________(��K1��K2��ʾ)
��2��ʵ���ҿ���NaOH��Һ����SO2��ijС��ͬѧ�������£���pH�������ⶨ��20mL0��1mol��L��1NaOH��Һͨ��SO2�����е�pH�仯������ͼ��ʾ��

��ab�η�����Ӧ�����ӷ���ʽΪ________________��
����֪d��ʱ��Һ������ΪNaHSO3����ʱ��Һ������Ũ���ɴ�С��˳��Ϊ_______�����NaHSO3��ˮ��ƽ�ⳣ��Kh=1��10-12mol��L��1������¶���H2SO3�ĵ�һ������ƽ�ⳣ��Ka=________________��
�ο��𰸣���p4��p3��p2��p1�����ȣ�1024mol2��L��2��
��1����867kJ��mol��1��K3=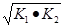
��2����SO2+2OH��=SO32��+H2O
��c(Na+)��c(HSO3��)��c(H+)��c(SO32��)��c(OH��)��
10��2mol��L��1
���������I.��ͼ��֪���¶Ƚ��ͣ�ת�����½������֪�÷�ӦΪ���ȷ�Ӧ����ӦCH4(g)+CO2(g) 2CO(g)+2H2(g)Ϊ�������ķ�Ӧ��ѹǿ����ƽ�����ƣ�����p4��p3��p2��p1��
2CO(g)+2H2(g)Ϊ�������ķ�Ӧ��ѹǿ����ƽ�����ƣ�����p4��p3��p2��p1��
CH4(g)+CO2(g) 2CO(g)+2H2(g)
2CO(g)+2H2(g)
ʼ 5mol 5mol 0 0
ת 4mol 4mol 8mol 8mol
ƽ 1mol 1mol 8mol 8mol
ƽ��Ũ�ȣ�0.5mol/L 0.5mol/L 4mol/L 4mol/L
���ԣ�K= =1024mol2/L2
=1024mol2/L2
II.��1��CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)��H1=��574kJ��mol��1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)��H2=��1160kJ��mol��1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)��H3
��ô��H3= =-867kJ/mol
=-867kJ/mol
���H3= ����ôK3=
����ôK3=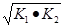
��2����20mL0��1mol��L��1NaOH��Һͨ��SO2���ɹ����е�pH�仯���߿�֪��a-b�η����ķ�Ӧ�Ƕ���������������Ʒ�Ӧ�����������ƣ������ӷ���ʽΪSO2+2OH��=SO32��+H2O��d��ʱ��Һ������ΪNaHSO3����Һ�����ԣ�����Ũ�ȵĴ�С��ϵΪ��c(Na+)��c(HSO3��)��c(H+)��c(SO32��)��c(OH��)����NaHSO3��ˮ��ƽ�ⳣ��Kh=1��10-12mol��L��1����Ka= =10-2mol/L��
=10-2mol/L��
���㣺��Ӧ�ȵļ��㣬ƽ�ⳣ���ļ��㣬���ӷ���ʽ����д������Ũ�ȴ�С�ıȽ�
�����Ѷȣ�����
4������� 32����16�֣�
��1����25�桢101kPa�£� 1g������ȫȼ������CO2��Һ̬H2O���ų�55 kJ��������д����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ�� ��
��2��2Zn��s��+O2��g��=2ZnO��s�� ��H1 =" ��702" kJ/mol
2Hg��l��+O2��g��=2HgO��s�� ��H2 =" ��182" kJ/mol
�ɴ˿�֪ZnO��s��+Hg��l��= Zn��s��+HgO��s�� ��H3= ��
��3����֪ 2SO2(g)+O2(g) =2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����֪1mol SO2(g)����Ϊ1mol SO3�Ħ�H=��99kJ��mol-1����ش��������⣺
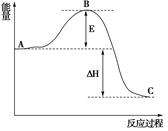
��ͼ��E��C�ֱ��ʾ �� ��
��E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ������Ӱ�죿 ���÷�Ӧͨ����V2O5����������V2O5��ʹͼ��B�������ǽ��ͣ� ��������
��ͼ�С�H= kJ��mol-1��
�ο��𰸣���1����� �� �����������
��2���ޣ����ͣ������ı��˷�Ӧ�����̣�ʹ���E���ͣ�
��3��-198
�����������1��1g����ȼ�շ���55 kJ��1mol������16g������Ϊ880 kJ��
��2����H =����-�٣�/2="+260" kJ/mol��
��3����ͼ��֪�÷�ӦΪ���ȷ�Ӧ��E���Ƿ�Ӧ�Ļ�ܣ�C���������������е��������ڷ�Ӧ�м��������ʹ��Ӧ�Ļ�ܽ��ͣ���H=2����-99 kJ��mol-1��="-198" kJ��mol-1��
���㣺�Ȼ�ѧ����ʽ�Ե���д����Ӧ�ȵļ���
������������Լ���Ҫ�������Ȼ�ѧ����ʽ�Ļ������㣬��˹���ɣ��Լ���ܵ�֪ʶ������ʱֻҪ��ͼ�������ɡ�
�����Ѷȣ�һ��
5������� ��1����֪��1mol H��H����1molN��H����1molN��N���ֱ���Ҫ��������436kJ��391kJ��946kJ����N2
��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ______________��
��2����֪���з�Ӧ�ķ�Ӧ��Ϊ��
��CH3COOH��l��+2O2��g��= 2CO2(g)+2H2O(l) ��H=- 870��3 kJ��mol-1
��C(s)+O2(g) = CO2(g) ��H=-393��5 kJ��mol-1
��H2(g)+O2(g) = H2O(l) ��H=-285��8 kJ��mol-1
�Լ������з�Ӧ�ķ�Ӧ�ȣ�2C(s)+2H2(g)+O2(g) = CH3COOH(l) ��H= __________��
�ο��𰸣���1��N2(g)+3H2(g) 2NH3(g) ��H=-92KJ/mol?
2NH3(g) ��H=-92KJ/mol?
��2�� -488.3KJ/mol
���������
�����Ѷȣ�һ��