| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《热化学方程式》高频考点特训(2017年练习版)(八)
参考答案: A 本题解析: ①中生成液态水放出的热量多,但ΔH为负值,所以ΔH1<ΔH2;②中ΔH1=2ΔH2<0;③中恒压条件下反应进行的程度大,放出的热量多;④中ΔH1>0,ΔH2<0。 本题难度:一般 2、选择题 已知:(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1 |
参考答案:B
本题解析:A、燃烧反应都是放热反应,所以△H1<0,错误;B、根据盖斯定律,2(2)+(3)-(1)即可得到(5)的热化学方程式,所以△H5=2△H2+△H3-△H1,正确;C、氢气在氧气中燃烧是放热反应,所以△H3<0,错误;D、若(1)-2(3)将得到(4)的逆反应的热化学方程式,所以△H4=-(△H1-2△H3),错误,答案选B。
考点:考查反应热的判断,盖斯定律的应用
本题难度:一般
3、选择题 含有NaOH 20.0 g的稀溶液与足量的稀盐酸反应,放出28.7 kJ的热量。能正确表示该反应中和热的热化学方程式是 ( )
A.NaOH +HCINaCI+H2O△H="-" 28.7 kj/mol
B.NaOH( aq)+HC1( aq)NaCl( aq)+H2O(1)△H="+57.4" kJ/mol
C.NaOH(1)+HCl(1)NaCl(l)+H2O(1)△H="-" 57.4 kJ/mol
D.NaOH( aq)+HCl( aq)NaCI( aq)+H2O(1)△H="-" 57.4 kJ/mol
参考答案:D
本题解析:首先,20.0gNaOH ,为0.5mol,1molNaOH 放出的热量为57.4kJ, NaOH( aq)+HCl( aq) NaCI( aq)+H2O(1)表示的为1mol的NaOH参加了反应.中和反应为放热反应,放热△H<0.相比较C选项,反应过程中参加反应的物质都以稀溶液的形式反应,所以为(aq)表示。水不能说是水的溶液,所以用l表示其液态水
本题难度:一般
4、填空题 (13分)研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为____________________________。利用反应6NO2+8NH3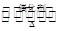 7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下的体积是________L。
7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下的体积是________L。
(2)已知:2SO2(g)+O2(g)  2SO3(g) ΔH="―196.6" kJ/mol ;
2SO3(g) ΔH="―196.6" kJ/mol ;
2NO(g)+O2(g)  2NO2(g) ΔH="―113.0" kJ/mol ;
2NO2(g) ΔH="―113.0" kJ/mol ;
①则反应NO2(g)+SO2(g)  SO3(g)+NO(g) ΔH 的ΔH=________。
SO3(g)+NO(g) ΔH 的ΔH=________。
②一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是___ _____。
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变
D.每消耗1 mol SO3的同时生成1 mol NO2
③测得上述反应平衡时NO2与SO2的体积比为1∶6,则平衡常数K=__ ______。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)  CH3OH(g) ΔH。CO在不同温度下的平衡转化率与压强的关系如图所示。
CH3OH(g) ΔH。CO在不同温度下的平衡转化率与压强的关系如图所示。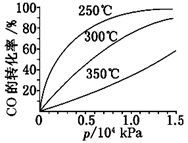
该反应ΔH________0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104 kPa左右,选择此压强的理由是______________________ 。
参考答案:(1)3NO2+H2O=2HNO3+NO(2分) 6.72(2分)
(2)①-41.8 kJ/mol(2分) ②B(2分) ③2.67或8/3(2分)
(3)<(1分) 在1.3×104 kPa下,CO转化率已较高,再增大压强,CO转化率提高不大,而生产成本增加,得不偿失(2分)
本题解析:(1)NO2溶于水生成硝酸和NO,反应的化学反应方程式为3NO2+H2O=2HNO3+NO。在反应6NO2+8NH3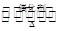 7N2+12H2O中,NO2中氮元素的化合价从+4价降低到0价,得到4个电子,因此如果转移1.2 mol电子时,消耗的NO2的物质的量是1.2mol÷4=0.3mol,在标准状况下的体积是0.3mol×22.4L/mol=6.72LL。
7N2+12H2O中,NO2中氮元素的化合价从+4价降低到0价,得到4个电子,因此如果转移1.2 mol电子时,消耗的NO2的物质的量是1.2mol÷4=0.3mol,在标准状况下的体积是0.3mol×22.4L/mol=6.72LL。
(2)①已知:I、2SO2(g)+O2(g)  2SO3(g) ΔH="―196.6" kJ/mol 、Ⅱ 2NO(g)+O2(g)
2SO3(g) ΔH="―196.6" kJ/mol 、Ⅱ 2NO(g)+O2(g)  2NO2(g) ΔH="―113.0" kJ/mol ,则根据盖斯定律可知(I―Ⅱ)÷2即得到反应NO2(g)+SO2(g)
2NO2(g) ΔH="―113.0" kJ/mol ,则根据盖斯定律可知(I―Ⅱ)÷2即得到反应NO2(g)+SO2(g)  SO3(g)+NO(g)的ΔH=-41.8 kJ/mol。
SO3(g)+NO(g)的ΔH=-41.8 kJ/mol。
②在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。A.反应前后体积不变,则压强始终不变,所以体系压强保持不变不能说明反应达到平衡状态,A错误;B.颜色深浅和浓度有关系,所以混合气体颜色保持不变可以说明反应达到平衡状态,B正确;C.根据方程式可知SO3和NO的体积比始终是1:1,所以比值保持不变不能说明反应达到平衡状态,C错误;D.根据方程式可知每消耗1 mol SO3的同时生成1 mol NO2,所以不能说明反应达到平衡状态,D错误,答案选B。
③ NO2(g)+SO2(g)  SO3(g)+NO
SO3(g)+NO
起始浓度(mol) 1 2 0 0
转化浓度(mol) x x x x
平衡浓度(mol)1―x 2―x x x
所以6×(1―x)=2―x
解得x=0.8
则平衡常数K=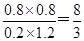
(3)根据图像可知在压强相同的条件下CO的转化率随着温度的升高而降低,这说明升高温度平衡向逆反应方向进行,即正方应是放热反应,所以该反应ΔH<0;
CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)  CH3OH(g) ΔH。CO在不同温度下的平衡转化率与压强的关系如图所示。”)。 根据图像可知在1.3×104 kPa下,CO转化率已较高,再增大压强,CO转化率提高不大,而生产成本增加,得不偿失,所以实际生产条件控制在250℃、1.3×104 kPa左右。
CH3OH(g) ΔH。CO在不同温度下的平衡转化率与压强的关系如图所示。”)。 根据图像可知在1.3×104 kPa下,CO转化率已较高,再增大压强,CO转化率提高不大,而生产成本增加,得不偿失,所以实际生产条件控制在250℃、1.3×104 kPa左右。
考点:考查盖斯定律、外界条件对平衡状态的影响、平衡状态判断、平衡常数计算等
本题难度:困难
5、选择题 相同温度下,有下列三个热化学方程式
(1)H2(g)+1/2O2(g)=== H2O(g) △H1= -Q1kJ・mol-1
(2)2H2(g)+O2(g)=== 2H2O(l) △H1= -Q2kJ・mol-1
(3)2H2(g)+O2(g)=== 2H2O(g) △H1= -Q3kJ・mol-1
则Q1、Q2、Q3的关系表示正确的是
[? ]
A.Q1=Q2<
B.Q2>Q3>Q1
C.Q3>Q2>Q1
D.Q1=Q2=Q3
参考答案:B
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点讲解《能量的相互.. | |