| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《物质的量》答题技巧(2017年最新版)(八)
参考答案:A 本题解析:A、N2和C2H4的摩尔质量相等,质量相等的N2和C2H4的物质的量相等,含有的分子数相同,正确;B、体积相同的N2和C2H4的分子数不一定相等,缺少等温等压条件,错误;C、等温、等体积的N2和O2,分子数不一定相同,缺少等压条件,错误;D.等压、等体积N2和CO2分子数不一定相同,缺少等温条件,错误。 本题难度:一般 3、选择题 对于相同质量的SO2和SO3,下列说法中正确的是( ) 参考答案:A、质量相同,SO2和SO3中硫元素的质量之比等于SO2和SO3中硫元素的质量分数之比为3264:3280=5:4,故A错误; 本题解析: 本题难度:简单 4、选择题 质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水,得到的溶液密度为q g/cm3(此过程中无溶质析出),物质的量浓度为c mol・L-1。则溶质的相对分子质量为 |
参考答案:C
本题解析:蒸发掉p g水后溶质质量分数为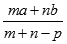 ,c=
,c=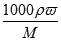 可知,溶质的摩尔质量M=
可知,溶质的摩尔质量M=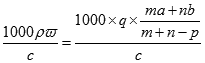 g/mol=
g/mol=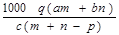 ,故答案为C.
,故答案为C.
考点:物质的量浓度的计算
本题难度:困难
5、填空题 (5分)(1)9.5gMgCl2固体溶于水配成500mL溶液,其浓度为?mol・L-1,从中取出100mL溶液,其中Cl-的物质的量为?mol;再把取出的溶液加水稀释成500mL,则此时MgCl2溶液的浓度为?mol・L-1。
(2).标准状况下将aLNH3气体溶于1L水中,所得盐酸溶液的密度为b g・cm-3,该溶液物质的量浓度是?mol・L-1。
参考答案:(5分)(1) 0.2? 0.04? 0.04?(2)?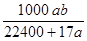 (2分)
(2分)
本题解析:(1)9.5gMgCl2是0.1mol,所以浓度是0.1mol÷0.5L=0.2mol/L;溶液是均一的,所以取出的溶液中浓度是不变的,因此根据化学式可知,氯离子浓度是0.2mol/L×2=0.4mol/L,物质的量是0.04mol;稀释过程中溶质是不变的,所以稀释后的浓度是0.2mol/L÷5=0.04mol/L。
(2)标准状况下。aL氨气的物质的量是a/22.4mol,质量是17a/22.4g。水的质量是1000g,所以溶液的质量是(1000+17a/22.4)g,则溶液的体积是(1000+17a/22.4)g÷bg/ml,因此根据c=n/V可知,氨气的浓度是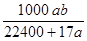
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点讲解《与量有关的.. | |