��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ʵ�����Na2O��Na2O2�ֱ�Ͷ�뵽�����ҵ�������ˮ�У��õ��������������ֱ�Ϊa����b����������Һ����a��b�Ĺ�ϵ��?��?��
A��a��b
B��a>b
C��a<b
D����ȷ��
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
2��ʵ���� (10��)8��34gFeS04��7H20��Ʒ������ˮ���̵���������(��Ʒ�������¶ȱ仯������)����ͼ��ʾ��
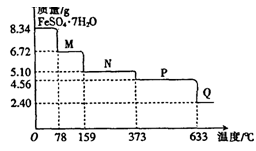
��ش��������⣺
(1)��ȷ��78��ʱ��������M�Ļ�ѧʽ��??��
(2)ȡ����380��ʱ���õ���ƷP����������������650�棬�õ�һ�ֹ�������Q��ͬʱ��������ɫ�������ɣ�д���÷�Ӧ�Ļ�ѧ����ʽ??
(3)ij��ȤС������ͼ��ʾװ�����ʵ�飬��֤(2)�����ɵ���̬���ʣ����ⶨ�ѷֽ��P������(������װ���ڿ�����Ӱ��)��

���Լ�X��������???��
�ڰ������������Ӹ�����������ĸ��ʾ�ӿڵ�����˳��c�� ?��
�۳�ַ�Ӧ������װ��III��Բ����ƿ�ڻ����ⶨ�ѷֽ��P�����������������Ϊ����һ������Բ����ƿ����μ����Ȼ�����Һ��ֱ��������ȫ���ڶ��������˻����ڹ������Ͻ�����ϴ����ɲ���ȴ�����£����ء���������������ɡ���ȴ������ֱ���������γ��������������0��1gΪֹ�������յõ�����������ΪWg�����ѷֽ��P������??(�����ʽ)?��
�ο��𰸣�
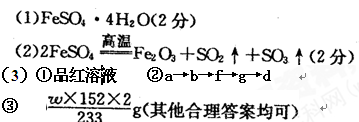
���������
��FeS04��7H20 FeSO4��XH2O��(7-x)H2O
FeSO4��XH2O��(7-x)H2O
278? 18(7�DX)
8.34? 8.34�D6.72
���X=4
FeS04��4H20
��2FeSO4 Fe2O3��SO2 ����SO3��
Fe2O3��SO2 ����SO3��
�Ǣ�Ʒ����Һ��a��b��f��g��d
��2FeSO4?~? SO3?~? BaSO4
2��152? 233
m? w

�����Ѷȣ�һ��
3��ѡ���� ���й��ڴ�����������������ǣ�������
A��Ӳ�ȱ�������
B�����������ᷴӦ
C�������Ũ�����жۻ�
D���ڸ���Ŀ����в�������
�ο��𰸣�A���Ͻ��Ӳ�ȱ�����ɷֵĶ�������Ϊ���ĺϽ�����Ӳ�ȱ������ͣ���A��ȷ��
B���ɽ������˳���֪��Fe�����ᷴӦ�����Ȼ���������������B����
C�������£�Fe��Ũ���ᷢ���ۻ����������ܵ���������ֹ��Ӧ�Ľ�һ����������C��ȷ��
D���������������������⣬����ʪ�����������⣬��FeӦע���ڸ��ﻷ���У���D��ȷ��
��ѡB��
���������
�����Ѷȣ�һ��
4������� �������ڿ������ױ����������γɸ��ο��ȶ����ڡ����������[(NH4)2SO4?FeSO4?6H2O]��һ����Ҫ��ѧ�Լ���ʵ���ҿ��ô���Ƭ����ȡ��������泥��������£�
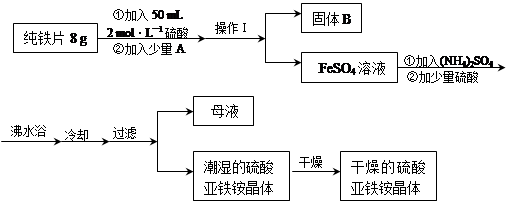
��ش��������⣺
��1��������������� ?��������Ҫ��������Ʒ�У�����̨����Ȧ���⣩?��
��2����A����ΪCuSO4��������Ŀ����??�������B�ijɷ�Ϊ?��
��3��������������Ե���pHΪ 1��2����������?��
�ο��𰸣���1�����ˣ�(1�֣� ��ֽ��©�������������ձ���1�֣�
��2���ӿ���Ƭ������ķ�Ӧ���ʣ�1�֣�������������Ҳ�ɣ�? Fe��Cu��2�֣�
��3������Fe2����NH4��ˮ�⣨2�֣�
�����������1����������������̷�����������Ϊ�����Һ�����IJ����������ǹ��ˣ�������Ҫ��������Ʒ�У�����̨����Ȧ���⣩��ֽ��©�������������ձ�����2����A����ΪCuSO4����������������Ӧ����ͭ������������������Һ���γ�ԭ��ط�Ӧ�ӿ���Ƭ������ķ�Ӧ���ʣ����˵õ�����B�ijɷ�Ϊ����ͭ�Ļ�����3��������������Ե���pHΪ 1��2����������������Ŀ���������������Ӻ�笠�����ˮ�⣬�õ�����IJ�Ʒ��
�����Ѷȣ�һ��
5��ѡ���� ����������Һ�У�����a?gͭ����ȫ�ܽ���ּ���b?g������ַ�Ӧ��õ�c?g������壬��b��c���������ж���ȷ���ǣ�������
A�����õ�����Һ�в�����Fe3
B������������Ϊ����ͭ�����
C�����õ�����Һ��ֻ��Cu2+
D���������һ��ȫ����ͭ
�ο��𰸣�AB
���������
�����Ѷȣ�һ��