| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《水的电离平衡》考点强化练习(2017年押题版)(二)
参考答案:C 本题解析: A、取NaOH溶液时仰视读数,会使氢氧化钠的体积偏多,造成消耗盐酸的体积偏多,测定结果偏高,错误;B、滴定结束后,滴定管尖嘴处有一悬挂液滴,对结果无影响,错误;C、锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度,会造成假滴定 终点的判断,使消耗盐酸的体积偏少,测定结果偏低,正确;D、盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2次~3次,会使氢氧化钠的体积偏多,造成消耗盐酸的体积偏多,测定结果偏高,错误,答案选C。 本题难度:一般 2、填空题 (10分)运用相关原理,回答下列各小题: 参考答案:(10分) 本题解析:(1)FeCl3是强酸弱碱盐,溶于水发生水解成酸性,即Fe3++3H2O 本题难度:一般 3、选择题 如图所示滴定前后滴定管中液面所处的刻度,则消耗溶液的体积为 |
参考答案:D
本题解析:滴定管的0刻度在上面,下面的读数较大,故所用体积(V2- V1)mL。
考点:滴定管的读数。
本题难度:一般
4、选择题 已知在常温下溶液中的pH+pOH=14,又已知正常人(人的体温高于室温)血液的pH=7.3,则正常人血液的pOH是
A.大于6.7
B.小于6.7
C.等于6.7
D.无法判断
参考答案:B
本题解析:常温下溶液中的pH+pOH=14,正常人(人的体温高于室温)血液的pH+pOH<14,所以正常人血液的pOH<6.7.
本题难度:困难
5、填空题 在a mL醋酸溶液中滴加0.01 mol・L-1的氢氧化钠溶液,滴定曲线如图所示。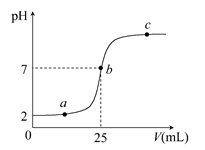
(1)醋酸溶液浓度________(填“大于”“小于”或“等于”)0.01 mol・L-1,理由是________;
(2)b点,c(Na+)________c(CH3COO-)(填“>”“<”或“=”)
(3)当醋酸与氢氧化钠溶液恰好完全中和时,曲线上对应的点Q应在____;
A.2与a之间 B.a与b之间
C.b与c之间 D.a与c之间
(4)下列关系式一定正确的是________。
A.a点,c(H+)>c(OH-)>c(CH3COO-)>c(Na+)
B.a点,c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.c点,c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.c点,c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
参考答案:(1)大于;CH3COOH是弱电解质,只部分电离
(2)= (3)C (4)D
本题解析:(1)开始时,醋酸溶液的pH=2,c(H+)=0.01 mol・L-1,由于醋酸是弱电解质,醋酸溶液中存在未电离的CH3COOH,故c(CH3COOH)>0.01 mol・L-1。(2)b点,pH=7表示c(H+)=c(OH-),由电荷守恒式c(Na+)+c(H+)=c(OH-)+c(CH3COO-)得出:c(Na+)=c(CH3COO-)。(3)CH3COOH+NaOH=CH3COONa+H2O,当醋酸与氢氧化钠恰好完全中和时,溶液呈碱性,pH>7,曲线上对应的Q点应在b与c之间。(4)a点,溶液的溶质是醋酸和醋酸钠,溶液显酸性,醋酸是弱酸,离子浓度大小关系为:c(CH3COO-)>c(H+)>c(OH-);无论溶液呈酸性、中性或碱性,其中都只存在Na+、H+、CH3COO-、OH-,所以一定有电荷守恒式,D选项正确。
本题难度:困难
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点归纳《元素周期律.. | |