微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (本题共14分)A、B、C、D 四种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
(1)B元素的名称:?;B在周期表中的位置第?周期,第?族;
(2)A、B形成的化合物为?化合物;(A.离子B.共价)
(3)C的元素符号:?,C的最高价氧化物的化学式:?;
(4) D的最高价氧化物对应的水化物的化学式:?。
参考答案:氮 2 五主 共价 S SO3? KOH
本题解析:A元素所处的周期数、主族序数、原子序数均相等,A为H;
B的最高价氧化物对应水化物的化学式为HBO3?,B最高价为+5,且B的原子半径是其所在主族中最小,B为N;
C元素原子的最外层电子数比次外层少2个,C为S;
C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C,D显+1,D为K;
本题难度:一般
2、选择题 下列比较中,正确的是
A.CH4与SiH4的稳定性:CH4>SiH4
B.HClO与H2SO4的酸性:HClO >H2SO4
C.1molHCl(g)的能量比1molH2(g)和1molCl2(g)的能量和高
D.Cl与S的原子半径:Cl >S
参考答案:A
本题解析:A.非金属性:C>Si;元素的非金属性越强,其对应的简单氢化物的稳定性就越强。故CH4与SiH4的稳定性:CH4>SiH4。正确。B.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强。非金属性:Cl>S,所以酸性:HClO4>H2SO4。错误。C.H2在Cl2中燃烧的反应是放热反应。所以2molHCl(g)的能量比1molH2(g)和1molCl2(g)的能量和低。错误。D.Cl与S是同一周期的元素。元素的原子序数越大,原子半径就越小。所以相应的原子半径:S>Cl。错误。
本题难度:一般
3、选择题 下列叙述正确的 (? )
A.同一周期的非金属元素,由左到右其氧化物对应水化物的酸性依次递增
B.aXn-与bYm+两种离子电子层结构相同,则b-a=n+m
C.同一主族非金属元素对应氢化物稳定性依次递增,是由于其相对分子质量依次递增、分子间作用力增强所导致的
D.同一主族非金属元素对应氢化物沸点由上到下依次递增
参考答案:B
本题解析:同周期自左向右,非金属性逐渐增强,最高价氧化物的水化物的酸性逐渐增强,A不正确;aXn-与bYm+两种离子电子层结构相同,这说明微粒的核外电子数是相等的,即b-a=n+m,B正确;氢化物的稳定性与非金属性强弱有关系,分子间作用力不是化学键,一般影响物质的物理性质,C不正确;D不正确,例如HF、H2O、NH3等分子间存在氢键,在同主族元素的氢化物中沸点最高,D不正确,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题贴近高考,难易适中。在注重对学生基础知识巩固和检验的同时,侧重对学生能力的培养。该题的关键是灵活运用元素周期律,其次注意氢键对物质性质的影响。
本题难度:一般
4、选择题 下列混合物的分离方法不正确的是
A.从酒精和水的混合物中分离出酒精――蒸馏法
B.使浑浊的食盐水变澄清――过滤法
C.从溴水分离出溴――分液法
D.把硝酸钾和氯化钾从同一溶液中分离出来――蒸发结晶法
参考答案:C
本题解析:A项酒精与水互溶为均匀的液态混合物;酒精的沸点比水的沸点低.应用蒸馏法可以把酒精从酒精与水的混合物中分离出来.
B项食盐水浑浊,说明食盐水里混有固体物质,过滤法可以除去混在液体里的固体物质,使液体由浑浊变澄清.
C项溴水是溴和水形成的均匀的液态混合物,分液法不能从溴水中分离出溴.要先用萃取剂(如四氯化碳、苯、汽油等)将溴从水中萃取出来,然后再进行分液.
D项硝酸钾和氯化钾都易溶于水;硝酸钾的溶解度受温度变化的影响较大,氯化钾的溶解度受温度变化的影响较小.因此,可以用蒸发结晶法把硝酸钾和氯化钾从同一溶液中分离出来.
本题难度:简单
5、简答题 (18分)(1)I.短周期某主族元素M的电离能情况如右图(A)所示。则M元素位于周期表的第?族。
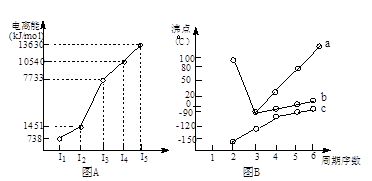
II.图B折线c可以表达出第?族元素氢化物的沸点的变化规律。两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:__________(填“a”或“b”)
III.部分有机物的熔沸点见下表:
烃
| CH4
| CH3CH3
| CH3(CH2)2CH3
| 硝基苯酚
| 
| 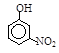
| 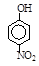
|
沸点/℃
| -164
| -88.6
| -0.5
| 熔点/℃
| 45
| 96
| 114
|
根据物质结构理论,由这些数据你能得出的相关结论是(至少写2条):
?,
?。
(2)COCl2俗称光气,分子中C原子采取?杂化成键;其中碳氧原子之间共价键含有?
?________(填字母):
a.2个σ键;b.2个π键;c.1个σ键.1个π键。
(3)金属是钛(22Ti) 将是继铜.铁.铝之后人类广泛使用的第四种金属,试回答:
I.Ti元素的基态原子的价电子层排布式为?;
II.已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体,其组成均为TiCl3・6H2O。为测定这两种晶体的化学式,设计了如下实验:a.分别取等质量的两种晶体的样品配成溶液;b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量发现产生的沉淀质量关系为:绿色晶体为紫色晶体的2/3。则绿色晶体配合物的化学式为?。
参考答案:(1)Ⅰ.ⅡA?Ⅱ. ⅣA? b?有机物分子量越大,分子间作用力越强,故沸点越高;当有机物能形成分子内氢键时,分子间作用力减弱,熔点变低;当分子间能形成氢键时,分子间作用力增强,熔点升高。(第一条必须写到,正确给2分;后两条任意写到1条均可,两条共4分)
(2)sp2? c?(3)Ⅰ.? 3d24s2 ?Ⅱ.[TiCl(H2O)5]Cl2?H2O 每空2分
本题解析:(1)Ⅰ.共计图像可知,A的第三电离能远大于第二电离能,所以A是第ⅡA元素。
Ⅱ.共计图像可知,折线c不是的氢化物的沸点逐渐升高,但都小于0℃。由于氨气、水、HF分子中都含有氢键,在该主族元素中沸点最高,所以c表示的是第ⅣA元素,其中b曲线是正确的,a曲线是错误的。
Ⅲ。根据三种烷烃的沸点可知,有机物分子量越大,分子间作用力越强,故沸点越高;由于邻硝基苯酚能形成分子内氢键,而对硝基苯酚内形成分子间氢键,所以根据硝基苯酚的熔点变化可知,当有机物能形成分子内氢键时,分子间作用力减弱,熔点变低;当分子间能形成氢键时,分子间作用力增强,熔点升高。
(2)光气是平面型结构,所以碳原子是sp2杂化。其中碳和氧形成的是碳氧双键,所以选项c正确。
(3)Ⅰ。根据构造原理可知,Ti元素的基态原子的价电子层排布式为3d24s2。
Ⅱ。由于作为配体的氯离子不能和硝酸银分液生成氯化银沉淀,所以根据所的沉淀的质量关系可知,绿色晶体配合物只有1个氯离子是配体,所以化学式为[TiCl(H2O)5]Cl2?H2O。
本题难度:一般