|
|
|
高中化学知识点总结《离子方程式的书写及正误判断》高频考点特训(2017年练习版)(一)
2017-09-25 17:02:55
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用1L1.0 mol・L-1NaOH溶液吸收0.8molSO2,所得溶液中的SO32-和HSO3-的物质的量浓度之比是
A.1:3
B.1:2
C.2:3
D.3:2
|
2、填空题 X、Y、Z三种物质有如下转化关系:

(1)根据上述转化关系,写出下列物质的化学式:
X 、Y 、Z ;试剂甲 ,试剂乙 。
(2)写出上述各步反应①~⑤的离子方程式:
① ;
② ;
③ ;
④ ;
⑤ 。
3、选择题 下列表示对应化学反应的离子方程式正确的是 ( )
A.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
B.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑
C.NH4HCO3溶于过量的NaOH溶液中:HCO―3+OH―=CO2-3+H2O
D.向氯化铝溶液中加入过量氢氧化钠溶液:Al3++4OH―=AlO―2+2H2O
|
4、填空题 (13分)铁、铜等金属及其化合物在日常生活中应用广泛,回答下列问题。
(1)工业上可用Cu2S+O2 2Cu+SO2。反应制取粗铜,当消耗32 g Cu2S时,转移电子的物质的量为____________________。
2Cu+SO2。反应制取粗铜,当消耗32 g Cu2S时,转移电子的物质的量为____________________。
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃-60℃,加入H2O2,反应一段时间后可制得硫酸铜,发生反应的离子方程式为:________________.CuSO4溶液中加入一定量的Na2SO3溶液和NaCI溶液加热,生成CuCl沉淀,写出生成CuCl的离子方程式________________________。
(3)电子工业常用30%的FeCl3溶液腐蚀附在绝缘板上的铜箔制造印刷电路板,取其腐蚀后的废液,加入一定量的铁粉后,若无固体剩余,则反应后的溶液中肯定有的离子是________________;若有红色固体,则反应后的溶液中肯定没有的离子是________,检验该离子的试剂为________。
(4)铁氰化钾 K3[Fe(CN)5]和亚铁氰化钾K4[Fe(CN)6] 的混合溶液可用于太阳能电池的电解液,该太阳能电池的工作原理示意图如图所示,其中催化剂a为________极,电极反应式为________;

5、填空题 (12分).铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层,铅在元素周期表的位置为 ,
PbO2的酸性比CO2的酸性 (填“强”或“弱”)。
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为 。
(3)PbO2可由PbO与次氯酸钠溶液反应制得反应的离子方程式为 ;
PbO2也可以通过石墨为电极Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取。阳极发生的电极反应式为_ _。若电解液中不加入Cu(NO3)2,主要缺点是 。
(4)PbO2在加热过程发生分解的失重曲线如下图所示,已知失重曲线上的a点为样品失重4.0%(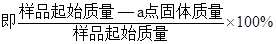 )的残留固体,若a点固体组成表示为PbOX或mPbO2・nPbO,列式计算x值和m:n值_ 。
)的残留固体,若a点固体组成表示为PbOX或mPbO2・nPbO,列式计算x值和m:n值_ 。
 2Cu+SO2。反应制取粗铜,当消耗32 g Cu2S时,转移电子的物质的量为____________________。
2Cu+SO2。反应制取粗铜,当消耗32 g Cu2S时,转移电子的物质的量为____________________。
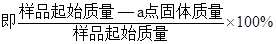 )的残留固体,若a点固体组成表示为PbOX或mPbO2・nPbO,列式计算x值和m:n值_ 。
)的残留固体,若a点固体组成表示为PbOX或mPbO2・nPbO,列式计算x值和m:n值_ 。