微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (18分)运用化学反应原理研究氮、氯等单质及其化合物的反应有重要意义。
(1)科学家研究在一定条件下通过下列反应制备NH3:
①在其他条件相同时,反应中NH3的体积分数(a)在不同温度下随反应时间(t)的变化如图。该反应的平衡常数表达式K=______,该反应中的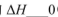 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
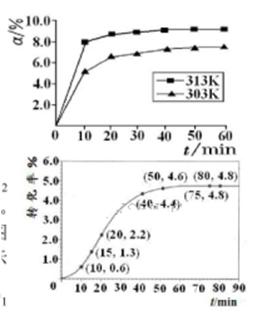
②某温度下,在2L容积不变的密闭容器中加入1molN2和6molH2O(1)发生反应,N2转化率随时间(t)变化如图。15-20min内,v(NH3)=____。若其他条件不变,在图中画出使用催化剂后N2的转化率随反应时间变化的曲线示意图。
(2) 25℃时,某同学将0.lmol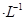 盐酸与0.2 mol
盐酸与0.2 mol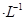 氨水等体积混合,所得混合溶液pH______7(填“>”“<”或“=”,下同),混合溶液中
氨水等体积混合,所得混合溶液pH______7(填“>”“<”或“=”,下同),混合溶液中 (25℃时,NH3.H2O的电离常数
(25℃时,NH3.H2O的电离常数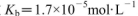 )
)
(3) 25℃时,向O.lmol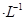 的MgCl2溶液中逐滴加入适量0.lmol
的MgCl2溶液中逐滴加入适量0.lmol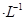 氨水,有白色沉淀生成,向反应后的浊液中,继续加入O.lmol
氨水,有白色沉淀生成,向反应后的浊液中,继续加入O.lmol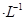 的FeCl3溶液,观察到的现象是______ ;上述过程中发生的所有反应的离子方程式为______。(25℃时,
的FeCl3溶液,观察到的现象是______ ;上述过程中发生的所有反应的离子方程式为______。(25℃时,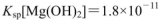 ,
,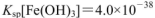 )
)
参考答案:(18分)
(1)①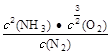 (2分)?>(2分)
(2分)?>(2分)
②0.0018mol・L-1・min-1(2分) 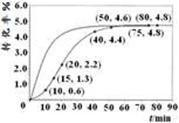
(2)>(2分)?>(2分)
(3)白色沉淀逐渐变成红褐色(2分)
Mg2++2NH3・H2O=Mg(OH)2↓+2NH4+(2分)
2Fe3+(aq)+3Mg(OH)2(s)=2Fe(OH)3(s)+3Mg2+(aq)(2分)
本题解析:(1)①根据平衡常数的含义,可得该反应的平衡常数K=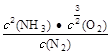 ;根据图像可知,温度升高,生成物NH3的体积分数逐渐增大,说明平衡向右移动,则该反应为吸热反应,?H > 0。
;根据图像可知,温度升高,生成物NH3的体积分数逐渐增大,说明平衡向右移动,则该反应为吸热反应,?H > 0。
②根据图像,15min时N2的转化率为1.3%,20min时N2的转化率为2%,则v(NH3)=2v(N2)=2×1mol×(2.2%-1.3%)÷2L÷5min=0.0018mol・L-1・min-1;使用了催化剂,反应速率加快,但平衡不移动,可画出曲线。
(2)0.l mol?L?1盐酸与0.2 mol?L?1氨水等体积混合,所得混合溶液含有等量的NH4Cl和NH3?H2O,溶液呈碱性,则pH > 7;NH3?H2O的电离程度大于NH4Cl的水解程度,所以c(NH4+)>c(NH3?H2O)。
(3)根据Mg(OH)2和Fe(OH)3的Ksp可知生成Fe(OH)3沉淀时OH?的浓度更小,所以Mg(OH)2沉淀会转化为Fe(OH)3沉淀;先后发生反应的离子方程式为:Mg2++2NH3・H2O=Mg(OH)2↓+2NH4+;2Fe3+(aq)+3Mg(OH)2(s)=2Fe(OH)3(s)+3Mg2+(aq)。
本题难度:一般
2、选择题 在一定温度不同压强(P1<P2)下进行的可逆反应2X(g) 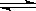 ?2Y(g) + Z(g),生成物Z 在反应混合物中的体积分数(ψ)与反应时间(t)的关系图正确的是(?)
?2Y(g) + Z(g),生成物Z 在反应混合物中的体积分数(ψ)与反应时间(t)的关系图正确的是(?)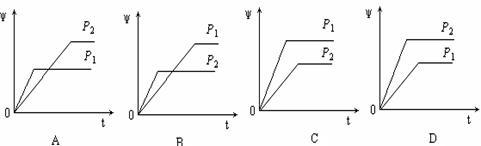
参考答案:B
本题解析:根据方程式可知,该反应是体积增大的可逆反应。所以增大压强,反应速率加快,但平衡向逆反应方向移动,Z的含量降低,因此选项B正确,答案选B。
点评:该题是基础性试题的考查,难度不大。该题侧重对基础性知识的巩固与训练,有助于调动学生的学习积极性,培养学生的应试能力。该题的关键是记住压强对反应速率和平衡状态的影响,然后结合反应和图像灵活运用即可。
本题难度:简单
3、选择题 已知图一表示的是可逆反应CO(g)+H2(g)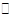 ?C(s)+H2O(g) ΔH>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)
?C(s)+H2O(g) ΔH>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)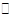 ?N2O4(g)ΔH<0的浓度(c)随时间(t)的变化情况。下列说法正确的是
?N2O4(g)ΔH<0的浓度(c)随时间(t)的变化情况。下列说法正确的是
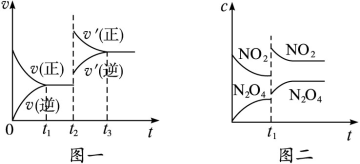
A.图一的t2时刻和和图二的t1时刻改变的条件都有可能是升高了温度或增大了压强
B.若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小
C.图一表示在新条件下达到平衡时,v′(正)>v′(逆),图二表示在新条件下达到平衡时,v′(正)<v′(逆)
D.其它条件不变,分别使用不同催化剂上述反应的平衡常数均不变
参考答案:D
本题解析: A、由2NO2(g) 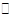 N2O4(g)中ΔH<0,升高了温度,平衡逆向移动,t1时刻后c(NO2)逐渐增大,c(N2O4)逐渐减小,错误;B、由
N2O4(g)中ΔH<0,升高了温度,平衡逆向移动,t1时刻后c(NO2)逐渐增大,c(N2O4)逐渐减小,错误;B、由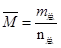 ,对反应2NO2(g)
,对反应2NO2(g)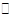 ?N2O4(g),增大压强,平衡正向移动,
?N2O4(g),增大压强,平衡正向移动,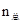 减小,
减小,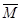 应该增大,错误;C、达到平衡时,v′(正)=v′(逆),错误;D、催化剂不改变平衡常数,正确。
应该增大,错误;C、达到平衡时,v′(正)=v′(逆),错误;D、催化剂不改变平衡常数,正确。
本题难度:一般
4、选择题 在一恒容的密闭容器中充入0.1 mol/L CO2、0.1 mol/L CH4,在一定条件下发生反应:CH4(g)+CO2(g)  2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是
2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是
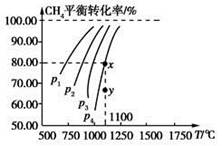
A.上述反应的ΔH<0
B.压强:p4>p3>p2>p1
C.1100 ℃时该反应平衡常数为1.64
D.压强为p4时,在y点:v正>v逆
参考答案:A
本题解析:本题考查了化学平衡,意在考查考生对化学平衡移动原理的理解及计算能力。由图像可知,压强一定时,温度越高,甲烷的平衡转化率越高,故正反应为吸热反应,ΔH>0,A项错误;该反应为气体分子数增加的反应,压强越高,甲烷的平衡转化率越小,故压强p4>p3>p2>p1,B项正确;1100 ℃时,甲烷的平衡转化率为80.00%,故平衡时各物质的浓度分别为c(CH4)=0.02 mol/L,c(CO2)=0.02 mol,c(CO)=0.16 mol/L,c(H2)=0.16 mol/L,即平衡常数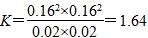 ,C项正确;压强为p4时,y点未达到平衡,此时v正>v逆,D项正确。
,C项正确;压强为p4时,y点未达到平衡,此时v正>v逆,D项正确。
本题难度:一般
5、选择题 在一定温度下,将等物质的量的CO和水蒸气通人恒容密闭容器中,发生如下反应:CO(g)+H2O(g)  ?CO2(g)+H2(g),一段时间后反应达到平衡。对该反应描述不正确的是
?CO2(g)+H2(g),一段时间后反应达到平衡。对该反应描述不正确的是
A.达平衡时CO的物质的量达到最小
B.此间CO2和 H2的浓度总是相等
C.未达平衡前正反应速率总是大于逆反应速率
D.若在CO中引入18O,则达平衡时,18O只可能存在于CO和CO2中
参考答案:D
本题解析:A正确,可逆反应达到平衡即为可逆反应所能达到的限度,即最大转化率,固平衡时反应物的浓度最小;B正确,根据化学反应方程式,CO(g)与H2O(g)以1:1形式反应,且起始加入的量也为1:1,所以CO2和 H2的浓度总是相等;C正确,未平衡前,反应总是向正反应方向进行,即平衡前正反应速率总是大于逆反应速率;D错,若在CO中引入18O,则达平衡时,18O可能存在于CO和CO2中和H2O(g)中。
本题难度:一般