| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ����ɡ�ԭ���ԭ�������㹮�̣�2017�����°棩(��)
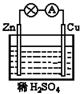 �ο��𰸣�A����ԭ����У�������п���ŵ�ʱ��пʧ���ӷ���������Ӧ����A���� ��������� �����Ѷȣ��� 3��ѡ���� һ������ȼ�ϵ�أ����Զ������Ϊ�缫����KOH��Һ�У�Ȼ��ֱ���������ͨ����(C2H6)����������缫��ӦʽΪ��C2H6+18OH����14e-=2CO32��+12H2O��2H2O+O2+4e-=4OH�����йش˵�ص��ƶϲ���ȷ����?(? )? �ο��𰸣�B �������������ԭ��ص�Ӧ�á���ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ������ϣ�������Һ�е��������������ƶ������������ƶ��������õ����ӣ�������ԭ��Ӧ�����Ը��ݵ缫��Ӧʽ��֪�����ڸ���ͨ�룬����������ͨ�룬AC��ȷ�����ݵ��ӵĵ�ʧ�غ��֪��������������ʵ���֮����7�U2�ģ�B����ȷ���������������缫��Ӧʽ��Ӽ��õ��ܷ�Ӧʽ2C2H6��7O2��8OH��=4CO32����10H2O������ѡ��D��ȷ����ѡB�� �����Ѷȣ�һ�� 4��ѡ���� ��ͼ��ʾװ���ܹ����ԭ���,�����ܲ������Ե�������(?) �ο��𰸣�B �������������ԭ��ص������ǻ����Բ�ͬ�Ľ���������ͷǽ������������������뵽�������Һ�У����B��ȷ��A�е缫��ͬ��C��û�й��ɻ�·��D���Ҵ����ǵ���ʣ���ѡB�� �����Ѷȣ�һ�� 5��ѡ���� п��������ؿ��ܳ�Ϊδ�������붯��Դ���õ�صĵ������Һ���������Ի���ԡ��ڼ�����Һ�иõ���ܷ�Ӧ�ɱ�ʾΪ��2Zn��4NaOH��O2=2Na2ZnO2 ��2H2O�������й�п���������˵����ȷ���� �ο��𰸣�D ���������A�����Ե������Һ������ӦΪO2�õ��ӣ�����B��������Һ��������ӦʽΪ��O2+4H++4e?=2H2O��������Һ��������ӦʽΪ��O2+H2O+4e?=4OH?��������Ӧʽ��ͬ������C���õ�ع���ʱ��Na����������������D��ZnԪ�ػ��ϼ���0��������+2�ۣ�����ÿ����1 mol ZnO22-ת�Ƶ�����Ϊ2NA����ȷ�� �����Ѷȣ�һ�� |
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ�ر�֪ʶ�㡶���ӹ��桷.. | |
| �����Ŀ |