微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
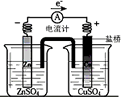
1、选择题 有关如下图所示原电池(盐桥中装有含琼胶的KCl饱和溶液)的叙述,正确的是
[? ]
A.铜片上有气泡逸出
B.取出盐桥后,电流计指针依然发生偏转
C.反应中,盐桥中的K+会移向CuSO4溶液
D.反应前后铜片质量不改变
2、选择题 下图各装置中,不能构成原电池的是 ( ) 
3、选择题 对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是(?)
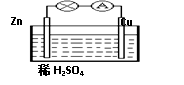
①Zn是负极?②电子由Zn经外电路流向Cu
③Zn-2e-=Zn2+?④溶液中H+向Zn棒迁移
A.①②
B.①②③
C.②③④
D.①②③④
4、填空题 某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因是________________
(2)实验室中现有Na2SO4、CuCl2、MgSO4、K2SO4等4种溶液,可与上述实验中CuSO4
溶液起相似作用的是________;
(3)要加快上述实验中气体产生的速率,还可采取的措施有________________(答两种)
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,
收集产生的气体,记录获得相同体积的气体所需时间。
实验
混合溶液
| A
| B
| C
| D
| E
| F
|
4mol/L H2SO 4/mL
| 30
| V1
| V2
| V3
| V4
| V5
|
饱和CuSO4溶液 /mL
| 0
| 0.5
| 2.5
| 5
| V6
| 20
|
H2O /mL
| V7
| V8
| V9
| V10
| 10
| 0
|
①请完成此实验设计,其中:V1= ,V6= ,V9= ;
② 该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
5、选择题 用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1 mol CuO后CuSO4溶液恰好恢复到反应前的浓度和pH。下列说法中不正确的是? ( )
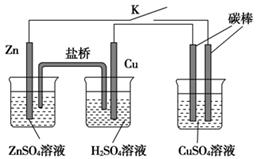
A.铜棒为正极,其电极反应式为:2H++2e-====H2↑
B.烧杯右侧碳棒为阴极,其电极表面有红色物质析出
C.反应中消耗锌的质量为13 g
D.导线中通过电子的物质的量为0.2 mol