微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各项中的两个量,其比例为2:1的是(?)
A.pH=7的氨水与(NH4)2SO4的混合溶液中,c(NH4+)与c(SO42-)之比
B.同温度下,0.2mol/LCH3COOH溶液与0.1mol/L CH3COOH溶液中的c(H+)之比
C.液面在“0”刻度,50mL酸式滴定管和25mL酸式滴定管内所盛溶液的体积
D.0.2mol/L的NaHSO3溶液中的阳离子与阴离子的浓度之比
2、填空题 重铬酸盐广泛用作氧化剂、皮革制作等。以铬矿石(主要成分是Cr2O3,含FeO、Al2O3、 SiO2等杂质)为原料制取重铬酸钠的流程如下:
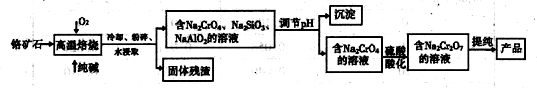
请回答下列问题:
(1)写出Cr2O3在高温焙烧时反应的化学方程式______________________
(2)写出硫酸酸化使Na-2CrO4转化为Na2Cr2O7的离子方程式 ______________。
(3)某工厂采用石墨电极电解Na2CrO4溶液,实 现了 Na2CrO4到? Na2Cr2O7的转化,其原理如图所示。

①钠离子交换膜的一种材料是聚丙烯酸钠(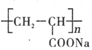 ),聚丙烯酸钠单体的结构简式是________;
),聚丙烯酸钠单体的结构简式是________;
②写出阳极的电极反应式__________
(4) Na2Cr2O7可用于测定废水的化学耗氧量(即COD,指每升水样中还原性物质被氧化 所需要O2的质量)。现有某水样100.00 mL,酸化后加入C1 mol/L的Na2Cr2O7溶液 V1 mL,使水中的还原性物质完全被氧化(Cr2O72-还原为Cr3+);再用C2mol/L的FeSO4溶液滴定剩 余的Cr2O72-,结果消耗FeSO4溶液V2 mL。
①该水样的COD为______________mg/L;
②假设上述反应后所得溶液中Fe3+和Cr3+的物质的量浓度均为0.1 mol/L,要使Fe3 +沉 淀完全而Cr3+还未开始沉淀.则需调节溶液pH的范围是 _______.
(可能用到的数据:KSPFe(OH)3=4.0×10-38, KSPCr(OH)3=6.0×10-31,
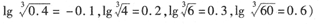
3、选择题 在BaSO3(s) 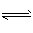 Ba2+(aq)+ SO32-(aq) 平衡体系中,下列措施可使沉淀量减少的是
Ba2+(aq)+ SO32-(aq) 平衡体系中,下列措施可使沉淀量减少的是
[? ]
A. 加入K2SO3(s)
B. 加入稀HNO3
C. 加入稀盐酸
D. 加入水
4、选择题 某温度下,Ag2SO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
A.a点表示Ag2SO4的不饱和溶液,加入Na2SO4固体可以使溶液由a点变到b点
B.a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到c点
C.0.04mol/L的AgNO3溶液与0.2mol/L的Na2SO4溶液等体积混合有Ag2SO4沉淀生成
D.Ag2SO4的溶度积常数(Ksp)为1×10-3