微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 工业制备白磷(P4)的方法很多,其中用得较多的方 法是以磷矿粉[Ca3(PO4)2]、焦炭(C)、石英砂(SiO2)为原料 制备白磷,其生产过程示意图如下: 请回答下列问题:

(1)试写出该法制备白磷的化学方程式:________________。
(2)已知断裂下列化学键需要吸收的能量分别为:P-P a kJ・mol-1;Cl-Cl b kJ・mol-1;P-Cl c kJ・mol-1。则反应: P4(s)+6Cl2(g)=4PCl3 (1) △H=_________。
(3)化学反应在反应物到生成物的过程中需经过一个高能量的过渡态(如图I),已知红磷的化学式为P,红磷和白磷充分 燃烧后的产物均为P4O10(温度高于300℃时易升华)。

①表示白磷燃烧热的热化学方程式为____。
②结合图I、Ⅱ分析,1 mol红磷完全转化为白磷,需____(填“吸收”或“放出”)的热量为______kJ。
2、选择题 由氢气和氧气反应生成1mol水蒸气放出241.8kJ的热量,1g水蒸气转化为液态水放出2.45kJ的热量,则下列热化学方程式书写正确的是( )
A.H2(g)+ O2(g)=H2O(l);△H=-285.9kJ/mol
O2(g)=H2O(l);△H=-285.9kJ/mol
B.H2(g)+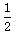 O2(g)=H2O(l);△H=-241.8kJ/mol
O2(g)=H2O(l);△H=-241.8kJ/mol
C.H2(g)+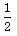 O2(g)=H2O(l);△H=+285.9kJ/mol
O2(g)=H2O(l);△H=+285.9kJ/mol
D.H2(g)+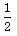 O2(g)=H2O(l);△H=+241.8kJ/mol
O2(g)=H2O(l);△H=+241.8kJ/mol
3、选择题 热化学方程式C(s)+H2O(g)
?CO(g)+H2(g);△H=+131.3kJ/mol表示( )
A.碳和水反应吸收131.3kJ能量
B.1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C.1mol固态碳和1mol水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ
D.1个固态碳原子和1分子水蒸气反应吸热131.1kJ
4、填空题 (8分).2009年10月16日第十一届全运会在济南举行,全运会使用的火炬的燃料是丙烷。
(1)已知11g丙烷完全燃烧生成CO2和液态水时放出的热量为555kJ,请写出丙烷燃烧热的热化学方程式
(2)某温度下,纯水中的c(H+)=2.0×10-7mol/L,若温度不变,滴入稀硫酸使c(H+)=5.0×10-6mol/L,则该溶液中由水电离出的c(OH-)为
5、简答题 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式是:______;
(2)PCl5分解成PCl3和Cl2的热化学方程式是:______;
上述分解反应是一个可逆反应.温度T1时,在密闭容器中加入0.80mol?PCl5,反应达平衡时PCl5还剩0.60mol,其分解率α1等于______;若反应温度由T1升高到T2,平衡时PCl5的分解率为α2,α2______α1(填“大于”、“小于”或“等于”);
(3)工业上制备PCl5通常分两步进行,现将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5.原因是______;
(4)P和Cl2分两步反应生成1mol?PCl5的△H?3=______,P和Cl2一步反应生成1mol?PCl5的△H?4______△H?3(填“大于”、“小于”或“等于”).
(5)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是:______.