��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��ҵ������Ĺ��������÷�Ӧ2SO2��g��+O2��g��
2SO3��g������H��0����SO2ת��ΪSO3��β��SO2����NaOH��Һ�������գ���ش��������⣺
��1��һ�������£���һ���������ܱ������г���2molSO2��1molO2������Ӧ��������˵����ȷ����______��
A������Ӧ����v��SO2����v��SO3���������˵���ÿ��淴Ӧ�Ѵﵽƽ��״̬
B�������¶Ⱥ�����������䣬����2molN2����ѧ��Ӧ���ʼӿ�
C��ƽ��������Ӧ��Ũ�ȣ���ƽ��һ�����ƣ�����Ӧ���ת����һ��������
D��ƽ����ƶ�����ѹ�����壬ƽ��ʱSO2��O2�İٷֺ�����С��SO3�İٷֺ�������
E��ƽ��������¶ȣ�ƽ�ⳣ��K����
F�������¶Ⱥ�����������䣬ƽ����ٳ���2mol SO3���ٴ�ƽ��ʱ�����Ũ�Ⱦ���ԭƽ��ʱ��Ũ�ȴ�
��2����һ������SO2��g����O2��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У��ڲ�ͬ�¶��½��з�Ӧ�õ����±��е��������ݣ�
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min
SO2
O2
SO2
O2
1
T1
4
2
x
0.8
6
2
T2
4
2
0.4
y
9
|
��ʵ��1�ӿ�ʼ����Ӧ�ﵽ��ѧƽ��ʱ��v��SO2����ʾ�ķ�Ӧ����Ϊ______������y��______��
��T1______T2����ѡ���������������=������ʵ��2�д�ƽ��ʱO2��ת����Ϊ______��
��3��β��SO2��NaOH��Һ���պ������Na2SO3�����г�����0.1mol/LNa2SO3��Һ��ʵ��ⶨ��pHԼΪ8������������⣺
�ٸ���Һ��c��Na+����c��OH-��֮��Ϊ______��
�ڸ���Һ��c��OH-��=c��H+��+______+______������Һ����������Ũ�ȱ�ʾ����
�۵������Һ�м�������NaOH����ʱ��c��SO32-��______��ˮ�����ӻ�Kw______����ѡ���������С�����䡱��
��4������ú������ʵ������ʵ����и���Һ�ֱ�������SO2���������������ɶൽ�ٵ�˳����______��
A��Na2CO3B��Ba��NO3��2C��Na2SD������KMnO4��
2��ѡ���� 700��ʱ�����ݻ�Ϊ2L���ܱ������г���һ������CO��H2O��������Ӧ��CO(g)+H2O(g)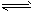 CO2+H2(g) ��Ӧ�����вⶨ�IJ������ݼ��±�������t1>t2��
CO2+H2(g) ��Ӧ�����вⶨ�IJ������ݼ��±�������t1>t2��
|

����˵����ȷ����
[? ]
A.��Ӧ��t1min�ڵ�ƽ������Ϊ��(H2)=0.40/t1 mol��L-1��min-1
B.���������������䣬��ʼʱ�������г���0.60molCO��1.20 molH2O������ƽ��ʱn(CO2)=0.40mol
C.���������������䣬��ƽ����ϵ����ͨ��0.20molH2O����ԭƽ����ȣ��ﵽ��ƽ��ʱCOת��������H2O�������������
D.�¶�����800�棬������Ӧƽ�ⳣ��Ϊ0.64��������ӦΪ���ȷ�Ӧ
3������� �ҹ��ǵ�һ��ú����ú��������ǣ�úȼ��ʱ���ͷų���������Ⱦ�Ի��������壬��NOx��SO2��CO2�ȡ������ȼú�����ʵ���������������ʵ����ɫ���������ܼ��ŵ�Ŀ�꣬�ֿɴﵽ���Ϊ������Լ��Դ��Ŀ�ġ�
(1)���ü������ԭNOx��
��CH4+4NO2=4NO+CO2+2H2O
��CH4+____NO=____+____CO2 +____H2O
�뽫��Ӧ�ڵĻ�ѧ����ʽ����������
(2)����NaOH��Һ�����շ����е�SO2��ij�������糧ÿ���ŷŵ�1. 12��104m3����״���£�β���к� 0.2%������ٷ�������SO2����������������Һ��ʯ�Ҽ���������������Ԫ�ز���ʧ�������Ͽɵõ�ʯ��(CaSO4��2H2O)__________kg��
(3)��CO2ת��Ϊ�״����Ȼ�ѧ����ʽΪ��CO2(g)+3H2(g) CH3OH(g)+H2O(g) ��H<0 ��һ���º����ܱ������г���1 mol CO2��3 mol H2������������Ӧ�����CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ��
CH3OH(g)+H2O(g) ��H<0 ��һ���º����ܱ������г���1 mol CO2��3 mol H2������������Ӧ�����CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ��

��0��3min�ڣ�v(H2)=_______
�ڸ������·�Ӧ��ƽ�ⳣ��Ϊ________
�۴ﵽƽ��ʱ������������������������ѹǿ��ƽ�ⳣ��______�����������С�����䡱����
4��ѡ���� 2008�������˻�ǰ������������̨�˻�������˫�����еĴ�ʩ�����������õ����Ը��ơ���֪NO��CO��������β���е���Ҫ�к����ʣ������ܻ����ط�Ӧ����N2��CO2��NO��CO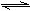 N2��CO2���йظ÷�Ӧ������������ȷ���ǣ�?��?
N2��CO2���йظ÷�Ӧ������������ȷ���ǣ�?��?
A��ʹ�ô������ܸı䷴Ӧ����
B������ѹǿ�к�����ת���ij̶�����
C���ı�ѹǿ�Է�Ӧ������Ӱ��
D�������¶�ʹ��Ӧ���ʼӿ�
5��ѡ���� 2SO2��g��+O2��g��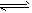 ?2SO3��g�����Ʊ��������Ҫ��Ӧ������������ȷ����
?2SO3��g�����Ʊ��������Ҫ��Ӧ������������ȷ����
[? ]
A������V2O5���ı�÷�Ӧ���淴Ӧ����
B������Ӧ��ϵ��ѹǿ����Ӧ����һ������
C���÷�Ӧ�Ƿ��ȷ�Ӧ�������¶Ƚ����̷�Ӧ�ﵽƽ���ʱ��
D����t1��t2ʱ�̣�SO3��g����Ũ�ȷֱ���c1��c2����ʱ����t1��t2�ڣ�SO2��g�����ɵ�ƽ������Ϊ