微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将51.2 g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/L NaOH溶液完全吸收,发生的反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O;NO+NO2+2NaOH=2NaNO2+H2O。
则生成的盐溶液中NaNO2的物质的量为
A.0.4 mol
B.0.6 mol
C.0.8 mol
D.0.2 mol
2、计算题 实验室里用二氧化锰与浓盐酸反应 来制取适量的氯气。现用浓盐酸与二氧化锰反应,生成的氯气在标准状况时的体积为11.2升,(假设HCl全部参加反应)
来制取适量的氯气。现用浓盐酸与二氧化锰反应,生成的氯气在标准状况时的体积为11.2升,(假设HCl全部参加反应)
(M
 nO2+4HCl(浓)
nO2+4HCl(浓)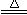 MnCl2+2H2O+Cl2↑)
MnCl2+2H2O+Cl2↑)
计算:(1)参加的二氧化锰的质量。?(2)被氧化的HCl的物质的量。
3、填空题 氮气及含氮的化合物在国民经济中占有重要地位。合成氨工业中,合成塔中每产生2 mol NH3,放出92.4 kJ热量。
(1)若起始时向容器内放入2 mol N2和6 mol H2,达平衡后放出的热量为Q,则Q 184.8kJ(填“>”、“<”或“=”)。一定条件下,在密闭恒容的容器中,能表示反应达到化学平衡状态的是 。
a.3v逆(N2)=v正(H2) b.2v正(H2)= v正(NH3)
c.混合气体密度保持不变 d.c(N2):c(H2):c(NH3)=1:3:2
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为
2NH3 (g)+ CO2 (g) CO(NH2)2 (l)+ H2O (l)。
CO(NH2)2 (l)+ H2O (l)。
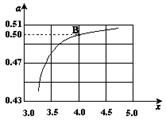
(2)在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)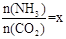 ,右图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的 原因是 。
,右图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的 原因是 。
(3)图中的B点处,NH3的平衡转化率为 。
(4)已知: 3Cl2+2NH3→N2+6HCl
4、填空题 高锰酸钾和浓盐酸可以发生下列反应:
2KMnO4+16HCl(浓)===5Cl2↑+2MnCl2+2KCl+8H2O
(1)该反应的氧化剂是___?___,还原剂是___?_____。
(2)若消耗0.2 mol氧化剂,则被氧化的还原剂的物质的量是________ mol。
5、填空题 (1)5molCO2的质量是______;在标准状况下所占的体积约为______;所含的分子数目约为______;所含氧原子的数目约为______.
(2)12.4gNa2X中含有0.4molNa+,则Na2X的摩尔质量是______,X的相对原子质量是______,该物质的化学式为______.
(3)有下列7种物质:Na2SO4、Na2SO3、K2SO4、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,请回答下列问题:
①将余下几种物质分别填入下面对应的横线上,组成一个未配平的化学方程式:
______+Na2SO3+______→Na2SO4+______+______+H2O
②反应物中发生氧化反应的物质是______(填化学式),被还原的元素是______.