微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某物质化学式为NH5,常温下为固体,能与水剧烈反应放出两种气体,且在NH5中的各原子均具有稀有气体的稳定结构,则下列有关NH5的描述中不正确的是(? )
A.组成NH5的元素都是非金属,属于共价化合物
B.NH5中氢元素为+1价
C.NH5与水的反应是氧化还原反应
D.NH5溶于水后溶液呈碱性
2、选择题 下列说法正确的是( )
A.凡是金属元素跟非金属元素化合都形成离子化合物
B.离子化合物中的阳离子都是金属离子
C.离子化合物中,一个阴离子可同时与多个阳离子之间有静电作用
D.溶于水可以导电的化合物一定是离子化合物
3、填空题 卤族元素的单质和化合物很多,请利用所学物质结构与性质的相关知识回答下列问题:
(1)卤族元素位于周期表的 ?区;氟原子的电子排布图为?溴原子的价电子排布式为?.
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是?
(3)已知高碘酸有两种形式,化学式分别为H5IO6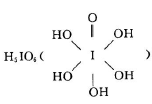 和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱: H5IO6??HIO4.(填“>”、“<”或“=”)。H5IO6中α键与π键的个数比为?。
和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱: H5IO6??HIO4.(填“>”、“<”或“=”)。H5IO6中α键与π键的个数比为?。
(4)碘在水中的溶解度虽然小,但在碘化钾溶液中溶解度却明显增大。这是由于溶液中发生下列反应 I-+ I2 =I3-与KI3类似的,还有CsICl2等。已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列 ?式发生。
A.CsICl2=CsCl+ICl? B.CsICl2 ="CsI" +Cl2
(5)ClO2-的空间构型为?型,中心氯原子的杂化轨道类型为?,写出一个ClO2-的等电子体 ?。
(6)如图为碘晶体晶胞结构。有关说法中正确的是?。

A.碘分子的排列有2种不同的取向
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘原子间存在非极性键和范德华力
(7)已知CaF2晶体(见图)的密度为ρg/cm3.NA为阿伏加德罗常数,相邻的两个Ca2+核间距为a cm,则CaF2的摩尔质量可以表示为?。
4、填空题 已知元素X、Y、Z、W、Q均为短周期元素,原子序数依次增大,X基态原子的核外电子分布在3 个能级,且各能级电子数相等,Z是地壳中含量最多的元素,W是电负性最大的元素,元素Q的核电荷数等于Y、W原子的最外层电子数之和。另有R元素位于元素周期表第4周期第Ⅷ族,外围电子层有2个未成对电子,请回答下列问题。
(1)微粒XZ32-的中心原子杂化类型为?化合物YW3的空间构型为?。
(2)R基态原子的电子排布式为?,元素X、Y、Z的第一电离能由大到小的顺序为
?(用元素符号表示)。
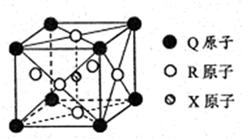
(3)一种新型导体晶体的晶胞如右图所示,则该晶体的化学式为?,其中一个Q原子紧邻?个R原子。
(4)R的氢氧化物能溶于含XY-离子的溶液生成一种配离子[R(XY)4]2-,该反应的离子方程式是?弱酸HXY分子中存在的σ键与 键的数目之比为?。
键的数目之比为?。
5、简答题 图中?A、B、C、D、E均为有机化合物.已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物.
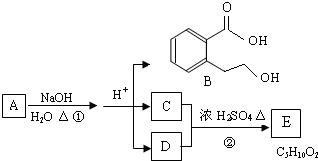
根据图回答问题:
(1)C分子中的官能团名称是:______;
下列反应中,化合物B不能发生的反应是______(填字母序号):
a、加成反应?b、取代反应?c、消去反应? d、酯化反应?e、水解反应?f、置换反应
(2)反应②的化学方程式是______.
(3)A的结构简式是______.
(4)同时符合下列三个条件的B的同分异构体的数目有______个.
Ⅰ.含有间二取代苯环结构;Ⅱ.属于非芳香酸酯;Ⅲ.与?FeCl3?溶液发生显色反应.
写出其中任意一个同分异构体的结构简式______
(5)常温下,将C溶液和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液pH如下表:
| 实验编号 | C物质的量浓度(mol?L-1) | NaOH物质的量浓度(mol?L-1) | 混合溶液的pH
m
0.1
0.1
pH=9
n
0.2
0.1
pH<7
|
从m组情况分析,所得混合溶液中由水电离出的c(OH-)=______mol?L-1.
n组混合溶液中离子浓度由大到小的顺序是______.