��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �������գ�
��1�������а������ʣ���MgCl2����ڸɱ���NaOH����ܰ��ף�P4������ݽ��ʯ�����壮�����������Ӿ������______�����ڷ��Ӿ������______������ԭ�Ӿ������______��
��2�������з��ӣ���CO2��NO2��SO3��BF3��NH3���������ڷǼ��Է��ӵ���______�����ӵ�VSEPRģ��Ϊƽ�������ε���______�����ڷ��ӵ����幹��Ϊ�����ε���______��
��3������ͬ�����£�SO2��ˮ�е��ܽ�Ⱥ�CO2��ˮ�е��ܽ����ȣ�SO2���ܽ�ȴ���ӷ������ʵĽǶȲ�������______
��4���ԱȽ�ͬ����Ԫ�ص��⻯��H2O��H2S��H2Se���ȶ��Ժͷе�ߵͣ���˵�����ɣ�
�ȶ��ԣ�______?���ɣ�______��
�е㣺______?���ɣ�______��
�ο��𰸣���1���������Ӿ�����ǣ�MgCl2���塢��NaOH���壻���ڷ��Ӿ�����ǣ��ڸɱ��ۡ��ܰ��ף�P4�����壻����ԭ�Ӿ�����ǣ��ݽ��ʯ�����壮
�ʴ�Ϊ���٢ۣ��ڢܣ��ݢޣ�
��2����CO2��Cԭ�ӵļ۲���Ӷ�Ϊ2��VSEPRģ��Ϊֱ���ͣ�û�й¶Ե��Ӷԣ�����Ϊֱ���ͶԳƽṹ�����ڷǼ��Է��ӣ�
��NO2��Nԭ�ӵļ۲���Ӷ�Ϊ52=2.5����3������VSEPRģ��Ϊƽ�������Σ�Nԭ����δ�ɼ��ĵ��ӣ�����ΪV�Σ����ڼ��Է��ӣ�
��SO3��Sԭ�ӵļ۲���Ӷ�Ϊ62=3��VSEPRģ��Ϊƽ�������Σ�Sԭ��û�й¶Ե��Ӷԣ�����Ϊƽ�������Σ��ṹ�Գƣ����ڷǼ��Է��ӣ�
��BF3��Bԭ�ӵļ۲���Ӷ�Ϊ3+1��32=3��VSEPRģ��Ϊƽ�������Σ�Bԭ��û�й¶Ե��Ӷԣ�����Ϊƽ�������Σ��ṹ�Գƣ����ڷǼ��Է��ӣ�
��NH3��Nԭ�ӵļ۲���Ӷ�Ϊ5+1��32=4��VSEPRģ��Ϊ�������壬Nԭ����1�Թ¶Ե��Ӷԣ�����Ϊ�����ͣ��ṹ���Գƣ����ڷǼ��Է��ӣ�
�����������ڷǼ��Է��ӵ��Ǣ٢ۢܣ����ӵ�VSEPRģ��Ϊƽ�������ε��Ǣڢۢܣ����ӵ����幹��Ϊ�����ε��Ǣݣ�
�ʴ�Ϊ���٢ۢܣ��ڢۢܣ��ݣ�
?��3��SO2��Sԭ�ӵļ۲���Ӷ�Ϊ62=3��VSEPRģ��Ϊƽ�������Σ�Sԭ��1�Թ¶Ե��Ӷԣ�����ΪV�Σ��ṹ���Գƣ����ڼ��Է��ӣ�CO2�ǷǼ��Է��ӣ�ˮ�Ǽ��Է��ӣ�������������ԭ����SO2��ˮ�е��ܽ�ȱ�CO2�Ĵ�
�ʴ�Ϊ��SO2�Ǽ��Է��ӣ�CO2�ǷǼ��Է��ӣ�ˮ�Ǽ��Է��ӣ�������������ԭ����SO2��ˮ�е��ܽ�ȱ�CO2�Ĵ�
��4���ǽ�����Խǿ����̬������Խ�ȶ����ǽ�����O��S��Se�������ȶ��ԣ�H2O��H2S��H2Se��
H2O���γɷ��Ӽ�������е���ߣ�H2Se��Է���������H2S���Ӽ������������H2Se��H2S�е�ߣ����Էе㣺H2O��H2Se��H2S��
�ʴ�Ϊ��H2O��H2S��H2Se���ǽ�����Խǿ����̬������Խ�ȶ����ǽ�����O��S��Se��
H2O��H2Se��H2S��H2O���γɷ��Ӽ�������е���ߣ�H2Se��Է���������H2S���Ӽ������������H2Se��H2S�е�ߣ�
���������
�����Ѷȣ���
2������� ��1���й��Ŵ��Ĵ���֮һ�����ڻ�ҩ�����ı�ը��ӦΪ��
2KNO3��3C��S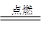 A��N2����3CO2��(����ƽ)
A��N2����3CO2��(����ƽ)
�ٳ�S�⣬����Ԫ�صĵ縺�ԴӴ�С����Ϊ?��
�����������У������Թ��ۼ��ķ��ӵ�����ԭ�ӹ���ӻ�����Ϊ_______�� A�ľ�������Ϊ____________��
����֪CN����N2�ṹ���ƣ�����HCN�����ЦҼ���м���Ŀ֮��Ϊ________________��
��2��ԭ������С��36��Ԫ��Q��T�������ڱ��мȴ���ͬһ������λ��ͬһ�壬��ԭ������T��Q��2��T�Ļ�̬ԭ����Χ����(�۵���)�Ų�Ϊ__________��Q2����δ�ɶԵ�������____________��
��3����CrCl3��ˮ��Һ�У�һ�������´������Ϊ[CrCln(H2O)6��n]x��(n��x��Ϊ������)�������ӣ�����ͨ�������ӽ�����֬(R��H)���ɷ������ӽ�����Ӧ��[CrCln(H2O)6��n]x����xR��H�D��Rx[CrCln(H2O)6��n]��xH��
����������H�����к͵ζ����������x��n��ȷ�������ӵ���ɡ�
����0.0015 mol [CrCln(H2O)6��n]x������Һ����R��H��ȫ�������к����ɵ�H����Ũ��Ϊ0.1200 mol��L��1NaOH��Һ25.00 mL����֪�������ӵĻ�ѧʽΪ?��
�ο��𰸣��𰸣�(1)��O>N>C>K����sp�ӻ�?���Ӿ��塡��1��1��(2)3d84s2��? 4��? (3)[CrCl(H2O)5]2��
���������(1)�ټ�Ϊ���ý������縺�Խ�С��C��N��O��ͬ���ڣ��ǽ���������ǿ���縺��Ҳ������K2S�����ӻ�����������Ӿ��壬�����к����Թ��ۼ��ķ���ΪCO2����ռ乹��Ϊֱ���Σ�����ԭ�ӹ���ӻ�����Ϊsp�ӻ�����HCN��CN����N2�ṹ��ͬ�����й���������һ���Ҽ��������м��������H֮���γ�һ���Ҽ�������HCN�����ЦҼ���м���Ŀ֮��Ϊ2��2����Ϊ1��1��
(2)ԭ������С��36��Ԫ��Q��T�������ڱ��мȴ���ͬһ������λ��ͬһ�壬Ӧ�ö����ڵڢ���Ԫ�أ�ԭ������T��Q��2������ȷ��TΪNi��QΪFe������T�Ļ�̬ԭ����Χ����(�۵���)�Ų�Ϊ3d84s2��Q2����Fe2����δ�ɶԵ�������4��
(3)�к����ɵ�H����Ũ��Ϊ0.1200 mol��L��1 NaOH��Һ25.00 mL������Եó�H�������ʵ���Ϊ0.1200��25.00��10��3��0.0030 (mol)������x��0.0030/0.0015��2��Cr�Ļ��ϼ�Ϊ��3�ۣ�x��2���Ե�n��1�����������ӵĻ�ѧʽΪ[CrCl(H2O)5]2����
�����������Ǹ߿��еij�����������ͣ������ۺ���ǿ�������߿���������ע�ػ���֪ʶ��ͬʱ�����ؿ���ѧ�������������ͽ��ⷽ����ѵ����ָ��������������ѧ���������������ͳ���˼ά���������ѧ���������⡢��������ͽ����������������������ѧ����Ӧ�����������ѧ����ѧϰЧ�ʺ�ѧϰ�����ԡ�
�����Ѷȣ�һ��
3��ѡ���� ���������мȺ��й��ۼ��ֺ������Ӽ�����(? )
A��NaI
B��CaCl2
C��NO2
D��KNO3
�ο��𰸣�D
���������NaIֻ�����Ӽ���CaCl2ֻ�����Ӽ���NO2ֻ�����Լ���KNO3�������Ӽ��ͼ��Լ���
�����Ѷȣ���
4��ѡ���� ��1molPԭ���γɵİ����к���P��P��Ϊ��NAΪ���ϳ�����
A��3NA? B��1.5 NA? C? 4 NA? D 0.25 NA
�ο��𰸣�B
�����������
�����Ѷȣ���
5��ѡ���� ���������У����ڹ��ۻ�������ǣ�������
A��NH4Cl
B��H2SO4
C��NaCl
D��I2
�ο��𰸣�B
���������
�����Ѷȣ���