微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组物质中,能用酸性高锰酸钾溶液鉴别的是(?)
A.乙烯、乙炔
B.己烷、苯
C.己烯、苯
D.苯、溴苯
参考答案:C
本题解析:乙烯和乙炔都可以使酸性高锰酸钾溶液褪色,不能鉴别,A错误;己烷和苯都不与酸性高锰酸钾溶液反应,不能鉴别,B错误;己烯可以使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色,可以鉴别,C正确;苯和溴苯不能使酸性高锰酸钾溶液褪色,D错误;所以答案选C。
本题难度:简单
2、选择题 实验室制取下列气体的实验正确的是
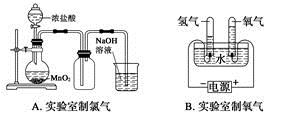
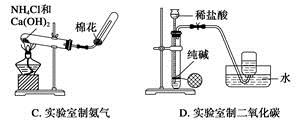
参考答案:C
本题解析:A项,实验室用MnO2和浓HCl反应制Cl2,需加热,错误;B项,实验室制O2不能用电解水的方法,错误;D项,纯碱易溶于水,不能控制反应的进行,错误。
本题难度:一般
3、填空题 (10分)某铝合金(硬铝)中含有镁、铜、硅,为了测定该合金中铝的含量,有人设计如下实验:
(1)取样品a g。
(2)将样品溶于足量稀盐酸中,过滤,滤液中主要含有的金属阳离子为________;滤渣中含有的物质为____________;
(3)往滤液中加入过量NaOH溶液,过滤,写出该步操作中与铝的化合物有关的离子方程式_____________________________。
(4)在第(3)步的滤液中通入足量CO2,过滤,将沉淀用蒸馏水洗涤数次后,烘干并灼烧至重量不再减少为止,冷却后称量,质量为b g。写出足量CO2通入滤液中所涉及的化学方程式________________。
(5)计算:该样品中铝的质量分数的表达式为___________________________。
参考答案:(10分) 1.(2)Mg2+、Al3+ (2分)? Cu、Si (2分)
(3) Al3++3OH-===Al(OH)3↓,Al(OH)3+OH-===AlO2-+2H2O
或Al3++4OH-=AlO2-+2H2O?(2分)
(4)NaAlO2+CO2+2H2O===NaHCO3+Al(OH)3↓?(2分)(5) 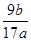 ×100%?(2分)
×100%?(2分)
本题解析:(2)单质铜和硅与盐酸不反应,所以将样品溶于足量稀盐酸中,过滤,滤液中主要含有的金属阳离子为Mg2+、Al3+,滤渣中含有的物质为Cu、Si。
(3)由于氢氧化铝是两性氢氧化物,所以往滤液中加入过量NaOH溶液,生成氢氧化镁白色沉淀,而铝离子先生成氢氧化铝白色沉淀,然后又溶解,反应的离子方程式分别是Al3++3OH-===Al(OH)3↓,Al(OH)3+OH-===AlO2-+2H2O或Al3++4OH-=AlO2-+2H2O。
(4)偏铝酸钠能和CO2反应生成氢氧化铝白色沉淀,由于CO2过量,所以反应的化学方程式是NaAlO2+CO2+2H2O===NaHCO3+Al(OH)3↓。
(5)最终生成的是氧化铝,质量是bg,则根据原子守恒可知,该样品中铝的质量分数的表达式为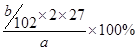 =
=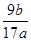 ×100%。
×100%。
点评:该题是中等难度的试题,试题贴近高考,难易适中,注重能力的培养和解题方法的训练,注重解题的灵活性。有利于培养学生的逻辑推理能力和发散思维能力,提高学生分析问题、解决问题的能力。有助于提高学生的应试能力和灵活应变能力。
本题难度:一般
4、实验题 (15分)氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成等都需要用到氯气。工业上通常采用电解法制氯气,其反应原理为:(用化学方程式表示)? ▲?。
某化学兴趣小组欲采用图一装置制取氯气,并探究氯气的性质。
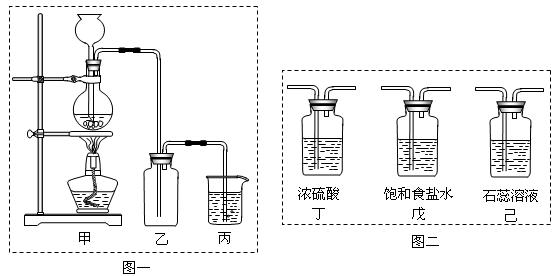
(1)指出图一装置中的错误之处? ▲??,? ▲?
(2)丙装置的作用? ▲?。丙装置中发生反应的离子方程式? ▲?。
(3)为了制得干燥纯净的Cl2,请你结合图二将以上装置重新排序:? ▲?。
(4)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是:
? ▲?。
A.NaBiO3
B.FeCl3
C.PbO2
D.Na2O2