微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列实验能成功的是 ?( ? )
A.将乙酸和乙醇混合加热制乙酸乙酯
B.用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热
C.CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型
D.苯和浓溴水反应制溴苯
参考答案:B
本题解析:A中还缺少浓硫酸和加热条件;C中溴乙烷不能电离出银离子,和硝酸银不反应;D中应该是液溴且还需要催化剂,所以正确的答案选B。
点评:该题是中等难度的试题,也是高考中的常见题型,试题难易适中,注重基础和能力的双向考查。有利于培养学生严谨、规范的实验设计和逻辑推理能力。
本题难度:简单
2、实验题 某化学实验小组为验证常见还原剂SO2、I-、Fe2+的还原性强弱的顺序为:
SO2>I->Fe2+,用下图所示装置进行实验(加热和夹持装置已略,气密性已检验)。
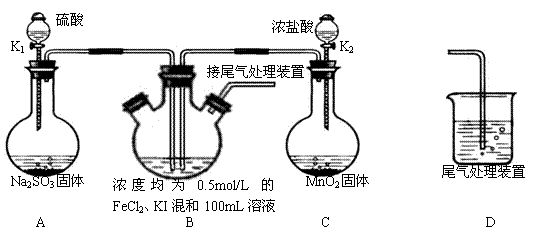
(1)上述实验需要加热的装置是
(2)D中,烧杯盛放的是
(3)实验开始时,关闭K1,打开K2,通入少量氯气,写出B中发生反应的离子方程式 ________________
①为验证I-的还原性比Fe2+强,取(3)后B中的少量溶液于试管中,应再往试管中滴入 ________ 溶液,现象是
②在(3)后,为了比较SO2和I-的还原性强弱,接下来的操作是
A.关闭K2开K1
B.关闭K1打开K2
C.同时打开K1和K2
(4)若打开K2,通入Cl2恰好将Fe2+、I-全部氧化后,再打开K1通入SO2,当Fe3+全部转化为Fe2+时,此时通入的SO2的体积(标准状况下)为 ?________?
参考答案:(13分 除第一空一分外其余每空二分)(1)C?(2)NaOH溶液
(3)2I-+ Cl2 =I2 + 2Cl-?淀粉溶液 溶液呈蓝色(或K(SCN)3溶液 溶液呈血红色)? A
(4)0.56L
本题解析:(1)实验室制备氯气需要加热,则需要加热的装置是C装置,答案选C。
(2)由于SO2和氯气都是大气污染物,需要尾气处理,所以D中烧杯盛放的氢氧化钠溶液。
(3)①由于碘离子的还原性强于亚铁离子,则氯气首先氧化的是碘离子,反应的离子方程式是2I-+ Cl2 =I2 + 2Cl- 。检验单质碘碘生成可以用淀粉溶液,实验现象是溶液呈蓝色。
②要比较SO2和I-的还原性强弱,则需要通过A装置制备SO2,所以正确的操作是关闭K2开K1,答案选A。
(4)碘离子和亚铁离子碘物质的量均是0.1L×0.5mol/L=0.05mol,通入SO2后,SO2分别将铁离子和单质碘还原为亚铁离子和碘离子,但由于铁离子的氧化性强于单质碘的,所以当Fe3+全部转化为Fe2+时,根据电子得失守恒可知,需要SO2的物质的量是0.05mol÷2=0.025mol,在标准状况下的体积是0.025mol×22.4L/mol=0.56L。2的制备、氧化还原反应的有关判断和计算、化学实验基本操作
点评:本题高考中的常见题型,属于中等难度的试题。试题基础性强,贴近高考,在注重对学生基础知识巩固和训练对同时,侧重对学生能力的培养,有利于培养学生规范严谨的实验设计能力和动手操作能力,也有助于提升学生的学科素养。
本题难度:一般
3、实验题 (14分)某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
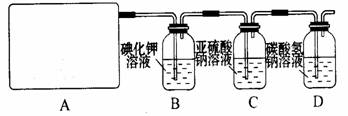
试回答:
(1)该实验中A部分的装置是 (填写装置的序号)。
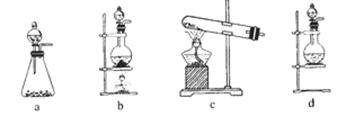
(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):
。
(3)若D中反应后的溶液具有漂白性,请写出D装置中发生反应的离子方程式? 。
(4)该实验存在明显的缺陷,请你提出改进的方法 。
(5)该小组又进行了如下实验:取漂白粉适量,研磨后溶解,配制成漂白液,运用下列实验,检测该漂白液的性质。
①将少量漂白液滴入含有淀粉的KI溶液中,溶液中出现蓝色;
②用pH试纸检测漂白液,试纸边缘为蓝紫色(pH=13),中间部分为白色;
③向漂白液中加入少量稀硫酸,溶液变为黄绿色,产生使湿润的淀粉KI试纸变蓝的气体。
请回答以下问题:
a、实验①表现出该消毒液具有 性;
b、实验②用pH试纸检测消毒液的操作是 _______________________;
c、实验③中涉及反应的离子方程式为 ____________;
参考答案:(14分)
(1)b
(2)取C中溶液少量,加入稀盐酸和氯化钡溶液,看是否产生沉淀
(3)Cl2+HCO3-=CO2+Cl-+HClO
(4)缺少尾气吸收装置
(5)a、氧化性;
b 、用干燥洁净的玻璃棒蘸取少量溶液,点在pH试纸上,并与标准比色卡对照读数;
c 、Cl-+ClO- +2H+=Cl2↑+H2O
本题解析:(1)实验室制氯气是固液加热装置,故选b
(2)Na2SO3被氧化为Na2SO4,故本题的目的是检验硫酸根离子的存在:取C中溶液少量,加入稀盐酸和氯化钡溶液,看是否产生沉淀
(3)也就是生成了HClO:Cl2+HCO3-=CO2+Cl-+HClO
(4)氯气有毒,一定要有尾气处理装置
(5)①证明有碘单质的生成,说明消毒液具有氧化性;
②基本的实验操作;
③有氯气的生成:Cl-+ClO- +2H+=Cl2↑+H2O
本题难度:一般
4、填空题 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯。回答下列问题:
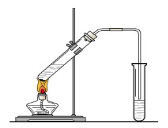
(1)写出制取乙酸乙酯的化学反应方程式: ? ?。
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法(加入试剂顺序)是:?。
(3)浓硫酸的作用是:①?;②?。
(4)饱和碳酸钠溶液的主要作用是?
?。
(5)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止? 。
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 ?
参考答案:(1)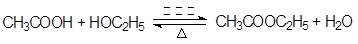
(2)先加乙醇,再缓慢滴加浓硫酸,最后滴加乙酸
(3)①催化剂;②吸水剂。
(4)中和乙酸,溶解乙醇,析出乙酸乙酯;
(5)防止倒吸,
(6)分液
本题解析:(1)在催化剂的作用下,乙酸和乙醇发生酯化反应生成乙酸乙酯,则该反应的化学方程式是 。
。
(2)由于浓硫酸的密度大于水的,且溶于水放热。又因为乙醇和乙酸都是挥发性的,所以加入试剂的先后顺序是先加乙醇,再缓慢滴加浓硫酸,最后滴加乙酸。
(3)在反应中浓硫酸起到催化剂的作用。又因为该反应是可逆反应,且有水生成,所以浓硫酸还起到吸水剂的作用。
(4)由于生成的乙酸乙酯中含有乙醇和乙酸,且乙酸乙酯不溶于水,所以饱和碳酸钠溶液的作用是中和乙酸,溶解乙醇,降低乙酸乙酯的溶解度,便于析出乙酸乙酯。
(5)由于生成的乙酸乙酯中含有乙醇和乙酸,而乙酸和乙醇与水都是互溶的,乙醇不能插入到溶液中的原因是防止倒吸。
(6)由于乙酸乙酯不溶于水,所以若要把制得的乙酸乙酯分离出来,应采用的实验操作是分液。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生实验能力的培养和解题方法的指导与训练,有助于培养学生规范、严谨的实验设计能力。该类试题主要是以实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。
本题难度:一般
5、填空题 为除去下表所列物质含有的少量杂质(括号内为杂质),在A项中选择试剂,在B项中选择操作的方法,将其代号填入表中:


A:(1)NaCl细颗粒;?(2)NaOH溶液;?(3)水;?(4)CaO;
(5)饱和Na2CO3;?(6)溴水;?(7)KMnO4溶液。
B:(1)过滤;?(2)盐析;?(3)蒸馏;?(4)分液;?(5)结晶;
(6)洗气;?(7)渗析
物质
| 蛋白质溶液
(氯化钠溶液)
| 乙?烷
(乙烯)
| 肥?皂
(甘油)
| 乙醇(水)
| 乙酸乙酯(乙酸)
| 溴苯(溴)
|
加入试剂
| ?
| ?
| ?
| ?
| ?
| ?
|
操作方法
| ?
| ?
| ?
| ?
| ?
| ?
参考答案:
物质
蛋白质溶液
(氯化钠溶液)
乙?烷
(乙烯)
肥?皂
(甘油)
乙醇(水)
乙酸乙酯(乙酸)
溴苯(溴)
加入试剂
(3)
(6)
(1)
(4)
(5)
(2)
操作方法
(7)
(6)
(2)
(3)
(4)
(4)
本题解析:略
本题难度:简单
|