微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)化合物A含硫(每个分子只含一个硫原子)、氧以及一种或几种卤素。少量A与水反应完全水解但不发生氧化或还原反应,所有反应产物均可溶于水。将A配成水溶液稀释后分成几份,分别加入一系列0.1mol/L的试剂,现象如下:
①加入硝酸酸化的硝酸银,产生白色沉淀;
②加入氯化钡溶液,无沉淀产生;
③溶液经酸化后加入高锰酸钾溶液,紫色褪去,再加入硝酸钡溶液,产生白色沉淀。
⑴由①判断组成该化合物的元素中,肯定存在的卤素有?,由②判断A与水反应后生成的溶液中肯定不存在的离子有? 。由③判断A与水反应后生成的溶液中肯定存在的离子有? .
。由③判断A与水反应后生成的溶液中肯定存在的离子有? .
⑵要确定该化合物的分子式,称取11.90gA溶于水稀释至250.00mL,取25.00mL溶液加入足量的高锰酸钾和硝酸钡溶液,使沉淀完全,沉淀经洗涤、干燥后称重为2.33g。试确定A的化学式,写出计算推理过程。
参考答案:⑴Cl;SO42―;?SO32― 或HSO3― 或SO32―、HSO3―都有;⑵SOCl2
本题解析:略
本题难度:一般
2、选择题 下列实验装置(固定装置略去)和操作正确的是( )
A.
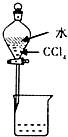
? 分离CCl4和水
B.
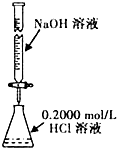
? 酸碱中和滴定
C.
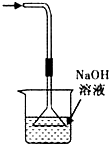
? 吸收HCl尾气
D.
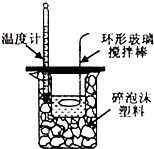
? 中和热的测定
参考答案:A
本题解析:
本题难度:一般
3、填空题 硼、镁及其化合物在工农业生产中应用广泛。
已知:硼镁矿主要成分为Mg2B2O5?H2O,硼砂的化学式为Na2B4O7?10H2O。利用硼镁矿制取金属镁及粗硼的工艺流程为:

回答下列有关问题:
(1)硼砂中B的化合价为?,溶于热水后,常用H2SO4调pH2~3制取H3BO3,反应的离子方程式为?。X为H3BO3晶体加热脱水的产物,其与Mg制取粗硼的化学方程式为?。
(2)MgCl2・7H2O需要在HCl氛围中加热,其目的是?。若用惰性电极电解MgCl2溶液,其阴极反应式为 ?。
(3)镁-H2O2酸性燃料电池的反应机理为Mg+H2O2+2H+==Mg2++2H2O,则正极反应式为??。若起始电解质溶液pH=1,则pH=2时溶液中Mg2+离子浓度为??。已知Ksp[Mg(OH)2]=5.6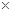 10-12,当溶液pH=6时??(填“有”或“没有”)Mg(OH)2沉淀析出。
10-12,当溶液pH=6时??(填“有”或“没有”)Mg(OH)2沉淀析出。
(4)制得的粗硼在一定条件下生成BI3,BI3加热分解可以得到纯净的单质硼。现将? 0.020g粗硼制成的BI3完全分解,生成的I2用0.30mol・L-1 Na2S2O3(H2S2O3为弱酸)溶液滴定至终点,消耗Na2S2O3溶液18.00mL。盛装Na2S2O3溶液的仪器应为?滴定管(填“酸式”或“碱式”)。该粗硼样品的纯度为 ?。(提示:I2+2S2O32-=2I-+S4O62-)
参考答案:(1)+3(2分) B4O72-+2H++5H2O= 4H3BO3(2分)Mg+B2O3===2B+3MgO(2分)?
(2)防止MgCl2水解生成Mg(OH)2(2分)?
2H2O+Mg2++2e-= H2↑+Mg(OH)2↓(2分)
(3)H2O2+2H++2e-=2H2O(2分)? 0.045 mol・L-1(2分)?没有(2分)
(4)碱式(2分)? 99%(2分)
本题解析:(1)根据硼砂的化学式Na2B4O7?10H2O和化合价的代数和为0,可得B的化合价为+3;B4O72-与2H+反应可得H3BO3,离子方程式为:B4O72-+2H++5H2O= 4H3BO3;X为H3BO3晶体加热脱水的产物,为B2O3,与Mg发生氧化还原反应,化学方程式为:Mg+B2O3===2B+3MgO。
(2)MgCl2为强酸弱碱盐,能发生水解反应,所以MgCl2・7H2O在HCl氛围中加热的目的是:防止MgCl2水解生成Mg(OH)2;用惰性电极电解MgCl2溶液,阴极反应为H2O电离出的H+放电,电解方程式为:2H2O+Mg2++2e-= H2↑+Mg(OH)2↓
(3)镁-H2O2酸性燃料电池的正极为H2O2放电,电极方程式为:H2O2+2H++2e-=2H2O;起始电解质溶液pH=1,pH=2时反应的H+为:0.1mol?L?1―0.01mol?L?1=0.09mol?L?1,根据Mg+H2O2+2H+==Mg2++2H2O,可得Mg2+离子浓度为0.045 mol・L-1;溶液pH=6时,c(OH?)=10-8mol?L?1,Q [Mg(OH)2]=" 0.045" mol・L-1×[10-8mol?L?1]2=4.5×10-18 < Ksp[Mg(OH)2],所以没有Mg(OH)2沉淀析出。
(4)Na2S2O3为强碱弱酸盐,水解显碱性,所以Na2S2O3溶液应盛放在碱式滴定管内;根据元素守恒和离子方程式可得:2B ~ 2BI3 ~ 3I2 ~ 6 S2O32-,所以粗硼样品的纯度为:0.018L×0.30mol?L?1×1/3×11g/mol÷×100% = 99%
本题难度:困难
4、选择题 36.5 g HCl气体体积是(?)
A.11.2 L
B.22.4 L
C.5.6 L
D.无法确定
参考答案:D
本题解析:36.5 g HCl气体状况(温度压强)未确定,所以无法确定其体积。
本题难度:简单
5、实验题 (9分)有如下两个反应(反应所需的其他条件和各物质的化学计量数均已略去):
①X+Y Z+P+Q;②Z+Q
Z+P+Q;②Z+Q X+H+Y。请针对以下两种不同情况来完成:
X+H+Y。请针对以下两种不同情况来完成:
(1)若X是一种日常生活中用作调味剂的盐,反应①是化学工业上制取单质Q和化合物Z的重要方法。则Z的电子式为___________________;反应①中阴极反应为___________________;反应②的离子方程式为______________;在酸性条件下,若将化合物H加到含Fe2+的溶液中,溶液从浅绿色变成黄色,该反应的离子方程式为_______________________________________。
(2)若X是一种含氧酸盐,可用于实验室中检验水的存在。1个X的酸根离子中共含有50个电子,其中含有一种元素R,R的原子最外层电子数是电子层数的2倍,则R在元素周期表中的位置是_________。X单质的熔点是112.8 ℃,则R单质的晶体类型属于______晶体。
(3)若X是(2)中的含氧酸盐,当以石墨作电极电解X溶液时,阳极反应为___________________;原溶液体积为1升,C(H+)=1×10-6mol/L。电解一段时间,当阳极收集到56ml(标况下)气体是,假定溶液体积不变,阴极棒将增重______g,此时电解质溶液的PH为_____。
参考答案:(1) ?;2H++2e-=H2↑;Cl2+2OH-====Cl-+ClO-+H2O
?;2H++2e-=H2↑;Cl2+2OH-====Cl-+ClO-+H2O
2Fe2++ClO-+2H+====2Fe3++Cl-+H2O
(2)第三周期第ⅥA族;分子
(3)4OH--4e-=2H2O+O2↑;0.64g;2(每空1分)
本题解析:(1)由“日常生活中用作调味剂的盐”可判断X是氯化钠,电解饱和食盐水是化学工业上制取氯气(Q)和氢氧化钠(Z)的重要方法,说明X是氯化钠的判断正确。氯气与氢氧化钠溶液反应生成次氯酸钠(H)、氯化钠(X)和水(Y),由于次氯酸钠是常见的强氧化剂,亚铁离子是常见的还原剂,根据“溶液从浅绿色变成黄色”判断氧化产物为铁离子,次氯酸根离子中的氯元素显+1价,得电子化合价降低,若降为0价生成的氯气可以氧化亚铁离子进一步降至-1价,因此次氯酸根离子的还原产物应为氯离子,根据得失电子守恒和电荷守恒就可以配平。
(2)实验室常用无水硫酸铜检验水的存在,1个硫酸根离子恰好含50个电子,其中的硫元素最外层电子数是6,电子层数是3,R为硫,位于元素周期表第三周期第ⅥA族。非金属单质硫的熔点较低可判断为分子晶体。
(3)通过第2小题分析明确了是电解硫酸铜溶液,则阳极电解氢氧跟。根据得失电子守恒算出阴极析出的铜的质量。而阳极电解了多少氢氧跟就可产生多少氢离子,从而算出电解后的PH
本题难度:一般