1、填空题
请根据反应 Fe + CuSO4=FeSO4 + Cu,设计原电池,完成以下问题。
负极:_______________ ,其电极反应式为:_______________________________
正极:_______________ ,其电极反应式为:_______________________________
电解质溶液:___________,电池的离子反应式为:_______________________________
参考答案:负极:Fe;其反应为:Fe-2e-==Fe2+;正极:Cu(其它正确的也可);其反应为:Cu2++2e-==Cu
电解质溶液:CuSO4;电池的离子反应为:Fe+Cu2+==Fe2++Cu
本题解析:
本题难度:一般
2、填空题 新型锂离子电池材料Li2 MSiO4(M为Fe,Co,Mn,Cu等)是一种发展潜力很大的电池电极材料。工业制备Li2 MSiO4有两种方法:
方法一:固相法,2Li2SiO3+ FeSO4 ?Li2FeSiO4 +Li2SO4 +SiO2
?Li2FeSiO4 +Li2SO4 +SiO2
方法二:溶胶―凝胶法,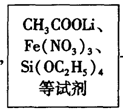
 Li2FeSiO4
Li2FeSiO4
(1)固相法中制备Li2 FeSiO4过程采用惰性气体气氛,其原因是?;
(2)溶胶―凝胶法中,检查溶液中有胶体生成的方法是?;生产中生成Imol Li2FeSiO4整个过程转移电子物质的量为?mol;
(3)以Li2 FeSiO4和嵌有Li的石墨为电极材料,含锂的导电固体作电解质,构成电池的总反应式为:Li+ LiFeSiO4 ?Li2FeSiO4则该电池的负极是____?;充电时,阳极反应的电极反应式为?;
?Li2FeSiO4则该电池的负极是____?;充电时,阳极反应的电极反应式为?;
(4)使用(3)组装的电池必须先____?。
参考答案:(11分)(1)防止Fe2+被氧化成Fe3+ (2分) ;?
(2)用一束强光照射溶液,从侧面能观察到一条光亮的通路。(2分);1mol (2分)
(3)嵌有Li的石墨(2分) Li2FeSiO4-e-=LiFeSiO4+Li+(2分) (4)充电(1分)
本题解析:(1)Fe2+具有还原性,故采用惰性气体气氛的原因是防止Fe2+被氧化成Fe3+。
(2)检查有无胶体生成,利用胶体的特征现象,即用一束强光照射溶液,从侧面能观察到一条光亮的通路。
(3)电池的负极失去电子、化合价升高,故负极是嵌有Li的石墨。阳极失去电子,化合价升高,电极式为Li2FeSiO4-e-=LiFeSiO4+Li+。
(4)使用(3)组装的电池必须先充电。
点评:本题考查的是锂电池的制备原理的信息题,题目难度大,利用好题中信息是解题的关键。
本题难度:一般
3、填空题 (11分)已知金属活动相差越大,形成原电池时越容易放电。请根据如图装置,回答下列问题:
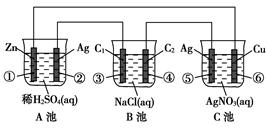
(1)各装置名称是:A池________,B池______,C池________。
(2)写出电极上发生的反应:①_____________,③___________,⑤_____________。
(3)当电路上有2 mol电子流过时,①极上质量变化______g,⑥极上质量变化______g。
(4)反应进行一段时间后,A、B、C三池中电解质溶液浓度不变的是________。
参考答案:(1)原电池 电解池 电镀池?(2)Zn-2e-==Zn2+ 2Cl--2e-==Cl2↑ Ag-e-==Ag+
(3)65 216 (4)C池
本题解析:由于两个电极活动性的差异最大的是Zn与Ag,所以A池是原电池。Zn是负极,发生氧化反应,Ag为正极,在正极上发生还原反应。相对其它池来说是电源。B池是电解池;C池是电解池。由于Ag电极与电源的正极连接,是阳极,Cu是与电源的负极连接的,是阴极。因此该池也就是电镀池。(2)①在Zn电极上发生反应: Zn-2e-==Zn2+;在③电极上Cl-放电,电极反应式是2Cl--2e-= Cl2↑;在⑤上由于Ag作阳极,所以是单质Ag失去电子,电极反应式是Ag-e-==Ag+。(3)当电路上有2 mol电子流过时,因为Zn是+2价的金属,所以有1mol的Zn发生氧化反应,所以①极上质量会减轻65g。在⑥极上会有质量变化2mol的Ag+得到电子,被还原,析出金属Ag,其质量为2mol×108g/mol=216g。(4)反应进行一段时间后,A池的电解质溶液会逐渐有H2SO4变为Zn SO4;B池会逐渐变为NaOH溶液;而在C池因为阳极产生Ag+离子,在阴极上是Ag+得到电子,被还原,所以仍然是AgNO3溶液, 浓度基本不变。选项为C。
本题难度:一般
4、选择题 下列有关说法正确的是
A.4CuO(s)=2Cu2O(s)-+O2(g)在室温下不能自发进行,说明该反应△H<0
B.生铁和纯铁同时放入海水中,纯铁更易腐蚀
C.常温下,PbSO4易溶于pH=7的CH3COONH4溶液,说明((CH3COO)2Pb是弱电解质
D.H2S(g)+FeO(s)  FeS(s)+H2O(g),其他条件不变时增大压强,反应速v(H2S)和H2S的平衡转化率均增大
FeS(s)+H2O(g),其他条件不变时增大压强,反应速v(H2S)和H2S的平衡转化率均增大
参考答案:C
本题解析:A、反应由固体转变生成气体,熵增加,若反应不能自发,则该反应一定是吸热反应,错误;B、生铁是铁和碳的混合物,两者构成原电池,在海水中的腐蚀快,错误;C、PbSO4与CH3COONH4反应生成(NH4)2SO4和Pb (CH3COO)2,(NH4)2SO4不是沉淀、也不是气体和弱电解质,但要满足复分解反应的条件,则Pb (CH3COO)2必须是弱电解质,正确;D、压强增加,反应速率加快,平衡向气体体积减小的方向进行,而该反应为等体积变化,故平衡不移动,错误。
本题难度:一般
5、选择题 控制合适的条件,将反应2Fe3++2?I- 2Fe2++?I2?设计成如图所示的原电池。下列判断不正确的是?
2Fe2++?I2?设计成如图所示的原电池。下列判断不正确的是?

[? ]
A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上Fe3+被还原
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中加入FeCl2固体,乙中石墨电极为负极
参考答案:D
本题解析:
本题难度:一般