1、选择题 为了确定某物质是否变质,所选试剂(括号内物质)达不到实验要求的是( )
A.K2SO3是否被氧化(BaCl2)
B.FeSO4是否被氧化(KSCN)
C.KI是否被氧化(淀粉溶液)
D.氢氧化钠是否被变质(BaCl2)
参考答案:A.K2SO3和K2SO4都能与BaCl2反应生成沉淀,不能用加入BaCl2的方法检验是否变质,应加入盐酸后在加入BaCl2,故A错误;
B.FeSO4被氧化生成Fe3+,Fe3+与KSCN反应,溶液为血红色,故B正确;
C.KI被氧化生成碘单质,加入淀粉变蓝色,故C正确;
D.氢氧化钠变质易生成Na2CO3,可加入BaCl2检验,故D正确.
故选A.
本题解析:
本题难度:简单
2、选择题 下列实验设计能完成或实验结论合理的是(?)
A.证明一瓶红棕色气体是溴蒸气还是二氧化氮,可用湿润的碘化钾―淀粉试纸检验,观察试纸颜色的变化
B.用核磁共振氢谱图鉴别1-丙醇和2-丙醇
C.测氯水的pH,可用玻璃棒蘸取氯水点在pH试红上,待其变色后和标准比色卡比较
D.铝热剂溶于足量稀盐酸再滴加KSCN溶液,未出现血红色,铝热剂一定不含Fe2O3
参考答案:B
本题解析:
正确答案:B
A.不正确,证明一瓶红棕色气体是溴蒸气还是二氧化氮,用湿润的碘化钾―淀粉试纸检验,观察试纸颜色的变化,均变蓝,无法鉴别;可有AgNO3溶液;
B.正确,用核磁共振氢谱图鉴别1-丙醇和2-丙醇,氢谱有三个峰的是2-丙醇,有四个峰的是1-丙醇
C.不正确,测氯水的pH,用玻璃棒蘸取氯水点在pH试红上,试纸会被漂白,应用pH计测。
D.不正确,Al+3Fe3+ =Al3++3Fe2+
本题难度:一般
3、实验题 下图是铜与稀硝酸反应的两个实验装置图,请回答下列问题:
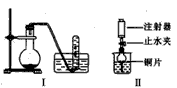
(1)铜与稀硝酸反应的离子方程式_____________________。
(2)I实验装置中能否证明铜与稀硝酸反应生成的是NO气体_____(填“能”或“不能”),简述理由___________________________。
(3)若用Ⅱ实验装置进行实验可证明铜与稀硝酸反应生成的气体是 _______________。在烧杯中加入一定体积的稀硝酸,打开止水夹,用注射器慢慢抽取干燥管内的空气,稀硝酸沿着干燥管慢慢上升,直到充满整个干燥管,停止抽拉注射器,关闭止水夹,观察干燥管内的现象_________________________。反应停止后,打开止水夹,用注射器抽取干燥管内的气体(事先已将注射器内原有的空气推出),关闭止水夹后取下注射器,并抽取一定量的空气,观察到的现象是_______________________________________。
(4)上述实验完成后,将注射器内的气体通入到NaOH溶液中,其目的是________________。
参考答案:(1)3Cu+8H++2NO3- = 3Cu2++2NO↑+4H2O
(2)不能;因烧瓶内有空气,用排水法收集时,NO与O2生成NO2,NO2又与水反应生成NO
(3)NO;铜片上产生大量无色气泡,管内液面下降,液面上有无色气体;无色气体立即变为红棕色
(4)防止氮的氧化物污染大气
本题解析:
本题难度:一般
4、实验题 一定量的浓H2SO4与足量的Zn充分反应时,有SO2和H2生成。某校化学研究性学习小组对此进行研究。

按图组装好实验装置,微热试管A,观察到C、D、E中均有气泡产生,随后气泡量减少,品红溶液褪色,D中先出现浑浊后浑浊消失;反应较长时间后,C、D、E中的气泡量又显著增加。试回答:
(1)装置A中需要用浓H2SO4,请用一种简单的方法确定一瓶H2SO4是浓H2SO4:_______________。
(2)从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接____、______接b,c接________、________接d。
(3)证明浓H2SO4具有强氧化性的实验现象为________________;反应较长时间后气泡又明显增加的原凶是________________。
(4)D中浑浊消失的离子方程式为_____________________。
(5)若要证明SO2具有还原性,C中的药品应该是_______________。
参考答案:(1)用火柴梗蘸取少量液体,若火柴梗立即变黑,证明是浓H2SO4(其他合理答案也可)
(2)3、4、2、1(或4、3、2、1)
(3)C中品红溶液褪色;浓H2SO4变为稀H2SO4后与 Zn反应放出H2
(4)SO2+H2O+CaSO3=Ca2++ 2HSO3-
(5)酸性KMnO4溶液或溴水
本题解析:
本题难度:一般
5、实验题 某校化学小组的同学开展K2CO3和NaCl的固体混合物中K2CO3的检验与质量分数测定的探究实验,他们提出下列实验方案。
(一)补全以下检验混合物中存在K2CO3的实验步骤及相关现象
(1)取混合物样品溶于水,分别取少量溶液进行以下实验
(2)_________________________________________则一定存在K+;
(3)___________________________________________________则一定存在CO32―。
(二)测定K2CO3质量分数
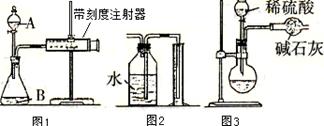
(1)甲同学用图1所示装置,把xg的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积。实验开始时检查该装置气密性的方法是?。
(2)乙同学用图2代替图1中的收集装置,则所测K2CO3质量分数??(填“偏大”、“偏小”、“不变”),你的改进方案是?。
(3)丙同学用图3装置测定CO2的质量,该装置存在较多缺陷,从而导致实验误差,请你填写其中的三点缺陷:I?;Ⅱ?;Ⅲ?
参考答案:(一)2.用焰色反应,同时透过钴玻璃片观看燃烧的火焰,如果是紫色的;
3.加入氯化钡溶液有白色沉淀,再加入盐酸沉淀溶解生成无色无味使澄清石灰水浑浊的气体。
(二)(1)关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位;
(2)偏小;将水换成饱和碳酸氢钠溶液;
(3):①产生的CO2气体中混有水蒸气,同时被碱石灰吸收,导致结果偏大;②反应结束后装置内残留的CO2气体不能全部排出,导致结果偏小;③球形干燥管与空气相通,也会吸收空气中的CO2和水蒸气,导致结果偏大;④实验开始时,装置内的空气中会有部分CO2也会被碱石灰吸收,导致结果偏大等。.
本题解析:(一)钾离子的检验一般用焰色反应,即用焰色反应,同时透过钴玻璃片观看燃烧的火焰,如果是紫色的,说明含有钾离子;CO32-的检验可以氯化钡和盐酸,即加入氯化钡溶液有白色沉淀,再加入盐酸沉淀溶解生成无色无味使澄清石灰水浑浊的气体。
(二)(1)由于有注射器,所以检查该装置气密性的方法是关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位;
(2)由于CO2能溶于水,造成收集的CO2体积减少,所以测定结果偏小;改正的方法是减少CO2的溶解,所以可将水换成饱和碳酸氢钠溶液。
(3)考查实验的评价,根据实验装置图即原理可知,存在的问题是①产生的CO2气体中混有水蒸气,同时被碱石灰吸收,导致结果偏大;②反应结束后装置内残留的CO2气体不能全部排出,导致结果偏小;③球形干燥管与空气相通,也会吸收空气中的CO2和水蒸气,导致结果偏大;④实验开始时,装置内的空气中会有部分CO2也会被碱石灰吸收,导致结果偏大等。
本题难度:一般