1、实验题 为研究铁质材料与热的浓硫酸的反应,某小组进行了以下探究活动:
【探究一】
(1)称取铁钉(碳索钢)12. 0 g放入30. 0 mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。
①甲同学认为X中除含有Fe3+外还可能有Fe2+。若要确认其中是否含有Fe2+,应选择加入的试剂为
_______(选填序号);
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取672 mL(标准状况)气体Y通入足量溴水中,发生反应SO2+Br2+2H2O =2HBr+H2SO4,然后 加入足量BaCl2溶液,得到4.66g沉淀,据此推知气体Y 中SO2的体积分数为_____________
【探究二】
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和CO2。为此设计了下列探究实验装置(图中央持仪器省略)。
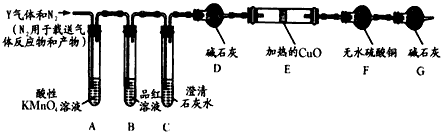
(2)写出产生CO2的化学方程式____________________
(3)装置A中试剂的作用是_________________
(4)简述确认气体Y中含有CO2的实验现象:____________________
(5)如果气体Y中含有H2,预计实验现象应是:______________________
2、实验题 已知亚甲基蓝( Methylene Blue)在碱性条件下与葡萄糖作用生成亚甲基白(Methylene White)。亚甲基蓝的结构如图所示。著名的“蓝瓶子实验”操作步骤如下:
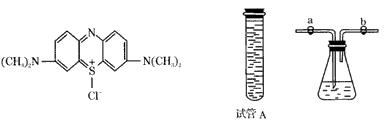
①如图所示,在250mL锥形瓶中,依次加入2g NaOH、100mLH2O、3gC6H12O6(葡萄糖),搅拌溶解后,再加入3~5滴2%的亚甲基蓝溶液,振荡后混合液呈现蓝色;
②关闭活塞a、b,塞紧橡皮塞,将溶液静置,溶液变为无色;
③再打开瓶塞,振荡,溶液又变为蓝色;
④关闭活塞a、b,再塞紧橡皮塞,将溶液静置,溶液又变为无色;
以上③、④操作可重复多次。
试回答:
(1)该实验中,影响溶液颜色互变快慢的主要因素有________。
(2)从上述变化的总结果看,葡萄糖的作用是____,亚甲基蓝的作用是____。
(3)上述实验中葡萄糖也可用鲜橙汁代替,因为其中含丰富维生素C,据此可推测维生素C具有____性。
(4)该实验中③、④操作能否无限次重复进行:____(填“能”或“不能”),理由是_____ 。
3、实验题 试用简单的实验证明,在醋酸溶液中存在着CH3COO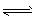 HCH3COO-+H+的电离平衡(要求写出简单操作、现象及实验能说明的问题)。
HCH3COO-+H+的电离平衡(要求写出简单操作、现象及实验能说明的问题)。
4、实验题 (14分)欲用浓硝酸法(测定反应后生成气体的量)测定某铜银合金中铜的质量分数。资料表明:①反应中除生成NO2气体外还有少量的NO生成;②常温下N02与N2O4混合存在,在低于0℃时几乎只有无色N2O4液体或晶体存在。为完成测定并验证有NO生成,有人设计下图实验装置。
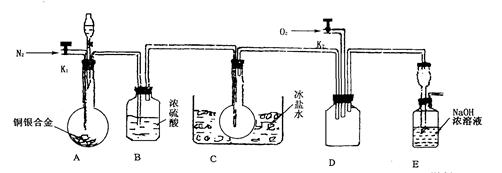
(1)实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是_____________________________________________________________。
(2)装置B瓶的作用是__________________________________________________。
(3)A中反应停止后,打开D中的活塞K2并通人氧气,若反应中确有NO产生,则D中应出现的现象是________________;实验发现,通人氧气温度的高低对实验现象有较大影响,则为了便于观察应通人_______________(填“冷”或“热”)的氧气。
(4)为了减少测量误差,在A中反应完成和D中出现现象后,还应继续进行的操作是__________________________________________________________。
(5)实验测得下列数据:所用铜银合金质量为15.0 g,浓硝酸的体积为40 mL,浓度为13.5mol・L-1。实验后:A中溶液体积为40mL,H+浓度为1.0mol・L-1。若设反应中硝酸既无挥发也无分解,则:
①参加反应的硝酸的物质的量为______________;
②若已测出反应后E装置的生成物含氮元素的质量,则为确定合金中铜的质量分数,还需要测定的数据是__________。
(6)实验中只测定铜的质量分数,不验证NO的产生,则在铜银合金与硝酸反应后,只需简单的实验操作就可以达到目的,请简述实验过程________________________。
5、选择题 以下是某学生利用集气瓶、导管、稀硫酸、四氯化碳一起设计的一套能“防止倒吸”,并能吸收氨气的装置。下列说法错误的是(?)

A.a为稀硫酸
B.b为四氯化碳
C.若吸收后的溶液中溶质为单一物质时,则不一定显酸性。
D.该吸收过程,表现了硫酸的酸性