1、实验题 氧化铜有多种用途,如作玻璃着色剂,油类脱硫剂等,为获得纯净的氧化铜以探究其性质,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:
(1)制备氧化铜
工业CuSO4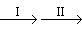 CuSO4溶液
CuSO4溶液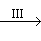 CuSO4・5H2O
CuSO4・5H2O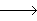 ……
…… 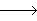 CuO
CuO
①步骤Ⅰ的目的是除不溶性杂质。操作是_____________ 。
②步骤Ⅱ的目的是除铁。操作是:滴加H2O2溶液,稍加热:Fe2+转化完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制溶液pH=3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1。滴加H2O2的目的是__________ ,加入Cu2(OH)2CO2粉末的目的是__________ 。
③步骤Ⅲ的目的是得到CuSO4・5H2O,操作是将CuSO4・5H2O 溶液加热蒸发至有晶膜出现时,停止加热,_____________,水浴加热烘干。 采用水浴加热的原因是________________ 。
(2)探究氧化铜性质
①取A、B两支试管,往A中先加入适量CuO粉末,再分别向A和B中加入等体积的3% H2O2溶液,只观察到A中有大量气泡,结论是____________ 。
②为探究试管A中反应的速率,收集气体并测定其体积必需的实验仪器除导管、橡皮塞、水槽外还必须有__________ 。
2、实验题 如下图所示,将浸透了石蜡油(17 个碳以上的液态烷烃混合物)的矿渣棉放在硬质玻璃管的底部,试管中加入碎瓷片,给碎瓷片加强热,石蜡油蒸汽通过炽热的碎瓷片表面发生反应。?
(1)若将生成的气体通入酸性高锰酸钾溶液后,溶液褪色并且液体分为两层,上层无色、油状,下层无色、水状。 ?
(2)若将生成的气体通入溴水,溴水也褪色。
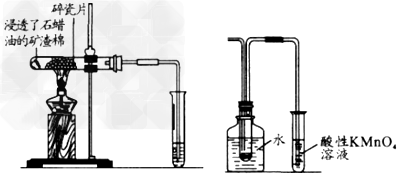
请回答下列问题: ?
(1)实验装置中矿渣棉的作用是____________,碎瓷片的作用是________。 ?
(2)酸性高锰酸钾溶液褪色,有机化合物发生的化学反应的类型是________。 ?
(3)溴水褪色,有机化合物发生的化学反应的类型是________,还能观察到的其他现象是
____________________。 ?
(4)若将生成的气体用上图所示的装置进行收集、检验,浸入水中的试管里形成了油状液体,另一试管内的酸性高锰酸钾溶液褪色。按上图所示的方法进行石蜡油裂化的实验,从实验安全性的角度来说,该实验设计中存在的主要问题是________________。 ?
(5)假设石蜡油中的某种烃的化学式是C18H38,它发生裂化反应生成了癸烷和烃A,癸烷又发生裂化反应生成了己烷和烃B,己烷又发生裂化反应生成了丁烷和烃C。写出上述裂化反应的化学方程式(有机化合物用化学式表示)。
①________________;②________________;③___________________。
3、实验题 (15分)食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
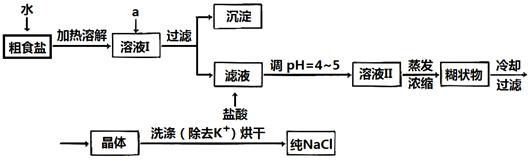
提供的试剂:饱和Na2CO3溶液?饱和K2CO3溶液? NaOH溶液? BaCl2溶液? Ba(NO3)2溶液? 75%乙醇 四氯化碳
①欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为_______? __(只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为_____?____。
(2)用提纯的NaCl配制500 mL4.00 mol・L-1NaCl溶液,所用仪 器除天平、药匙、玻璃棒外还有___?_____(填仪器名称)。
器除天平、药匙、玻璃棒外还有___?_____(填仪器名称)。
(3) 电解饱和食盐水的装置如图所示,

若收集的H2为2 L,?
则同样条件下收集的Cl2______(填“>”、“=”或“<”)2 L,原因是__________。装置改进后,可用于制备NaOH溶液,若测定溶液中NaOH的浓度,常用的方法是_____________。
(4)实验室制备H2和Cl2通常采用下列反应:Zn+H2SO4?ZnSO4+H2↑;MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,据此,从下列所给仪器装置中选择制备并收集H2的装置_______(填代号)和制备并收集干燥、纯净Cl2的装置_________(填代号)。
MnCl2+Cl2↑+2H2O,据此,从下列所给仪器装置中选择制备并收集H2的装置_______(填代号)和制备并收集干燥、纯净Cl2的装置_________(填代号)。
可选用制备气体的装置:
4、实验题 选做题
经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。
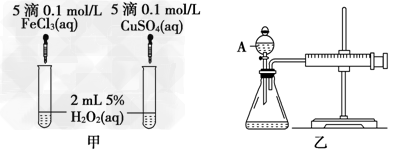
回答相关问题:
(1)?定性分析:如图甲可通过观察________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是__________________,写出H2O2在二氧化锰作用下发生反应的化学方程式 ________________________。 ?
(2)?定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为________,实验中需要测量的数据是________________。检查乙装置气密性的方法是___________________。
(3)?0.6?mol?X气体和0.6?mol?Y气体混合于2?L密闭容器中,发生如下反应: 2X(g)+Y(g)===nZ(g)+2W(g),?2?min末生成0.2?mol?W,若测得以Z的物质的量浓度变化表示的反应速率为0.1?mol/(L・min),则前2?min内,用X的物质的量浓度变化表示的平均反应速率为________;2?min末时Y的物质的量浓度为________;化学方程式中,Z的化学计量数n=________。
(4)?在一定温度下,反应:2A(s)+2B(g)?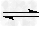 C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________?
C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________?
A.容器内的压强不随时间而变化 B.混合气的密度不再随时间而变化 C.A的质量不再改变? D.平衡混合气体的平均相对分子质量不再改变
5、实验题 (18分)实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO=3H++6H2O+(CH2)6N4H+[滴定时,1 mol (CH2)6N4H+与 l mol H+相当],然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ称取1.500 g样品,加水溶解,配成250 mL溶液。
步骤Ⅱ用酸式滴定管量取25.00 mL样品溶液于 250 mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液。用0.1010 mol・L-1的NaOH标准溶液滴定至终点。按上述操作方法再重复2次。?
250 mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液。用0.1010 mol・L-1的NaOH标准溶液滴定至终点。按上述操作方法再重复2次。?
⑴根据实验步骤填空:
①步骤Ⅰ中用到的主要玻璃仪器有?;
②步骤Ⅱ中酸式滴定管用蒸馏水洗涤后,直接加入样品溶液进行量取,则测得样品中氮质量分数?(填“偏高”、“偏低”或“无影响”,下同)。锥形瓶用蒸馏水洗涤后,水未倒尽,则对滴定时用去NaOH标准溶液的体积?。滴定时对NaOH标准溶液体积,读取初读数时仰视,读取终读数时姿势正确,则测得样品中氮质量分数?。
③滴定时边滴边摇动锥形瓶,眼睛应观察?
A.滴定管内液面的变化?
B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由?色变成?色。
⑵滴定结果如表所示:
滴定次数
| 待测溶液体积/ml
| 标准NaOH溶液体积读数(ml)
|
滴定前/ml
| 滴定后/ml
|
1
| 25.00
| 1.02
| 21.03
|
2
| 25.00
| 2.00
| 21.99
|
3
| 25.00
| 2.30
| 22.30
|
则消耗NaOH标准溶液的体积平均为?,该样品中氮的质量分数为?。