1、选择题 25 ℃、101 kPa下:①2Na(s)+O2(g)=Na2O(s)?;? ΔH1=-414 kJ/mol
②2Na(s)+O2(g)=Na2O2(s)?;? ΔH2=-511 kJ/mol?
下列说法正确的是
A.①和②产物的阴阳离子个数比不相等
B.①和②生成等物质的量的产物,转移电子数不同
C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D.25 ℃、101 kPa下,Na2O2(s)+2Na(s)=2Na2O(s) ; ΔH=-317 kJ/mol
2、选择题 取实验室中部分变质的NaOH样品配成溶液,向其中滴加稀盐酸,绘制出生成的CO2的质量与加入的盐酸的质量间的关系如图所示,下列有关说法正确的是
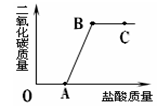
A.OA段没有发生任何反应
B.C点的溶液的pH=7
C.B点表示加入的盐酸与原溶液中的溶质恰好完全反应
D.C点溶液中的溶质只有NaCl
3、选择题 一定温度下,向饱和的NaOH溶液中加入少量的Na2O2固体,充分反应后恢复到原来的室温,下列叙述不合理的是?(?)
A.NaOH溶液浓度增大,并且放出O2
B.溶液的质量变小,有O2放出
C.NaOH的质量分数不变,有NaOH晶体析出
D.溶液中Na+的物质的量浓度不变,但物质的量减少了
4、选择题 下列各组物质混合后,不能生成NaOH的是
A.Na和H2O
B.Na2O2和H2O
C.Ca(OH)2溶液和Na2CO3溶液
D.Ca(OH)2溶液和NaCl溶液
5、实验题 某实验小组把CO2通入饱和Na2CO3溶液制取NaHCO3,装置如图所示(气密性已检验,部分夹持装置略):
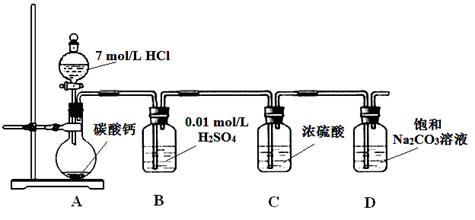
(1)D中产生NaHCO3的化学方程式是?。
(2)请结合化学平衡移动原理解释B中溶液的作用?。
(3)当D中有大量白色固体析出时,停止实验,将固体过滤、洗涤、干燥备用。为确定固体的成分,实验小组设计方案如下(称取一定质量的固体,配成1000 mL溶液作为样液,其余固体备用):
① 方案1:取样液与澄清的Ca(OH)2溶液混合,出现白色沉淀。
实验小组对现象产生的原理进行分析,认为该方案不合理,理由是 ?。
② 方案2:取样液与BaCl2溶液混合,出现白色沉淀并有气体产生。
实验小组认为固体中存在NaHCO3,其离子方程式是?。
该小组认为不能确定是否存在Na2CO3,你认为该结论是否合理?_____。
③ 方案3:实验小组中甲、乙同学利用NaHCO3的不稳定性进行如下实验:
甲同学:取样液400 mL,用pH计测溶液pH,再水浴加热蒸发至200 mL,接下来的操作是?,结果表明白色固体中存在NaHCO3。为进一步证明白色固体是否为纯净的NaHCO3,结合甲同学实验,还应补充的实验是?。
乙同学:利用仪器测定了固体残留率随温度变化的曲线,如下图所示。
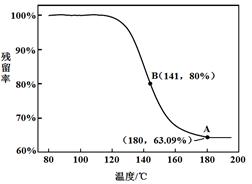
a. 根据A点坐标得到的结论是?。
b. 根据B点坐标,计算残留固体中n(NaHCO3:n(Na2CO3))=?。
通过上述实验,该小组认为,可以向饱和Na2CO3溶液中通入过量CO2制备NaHCO3。